25/01/2022
El acumulador de plomo, conocido popularmente como batería de plomo-ácido, es una tecnología fundamental que ha impulsado vehículos y sistemas de energía durante más de un siglo. Aunque su diseño ha evolucionado, el principio básico ideado hace mucho tiempo sigue siendo el núcleo de su funcionamiento. Es el tipo de batería más común en los vehículos convencionales, actuando como la vital fuente de energía para el arranque del motor, aunque también encuentra aplicaciones esenciales en vehículos eléctricos como batería de tracción.
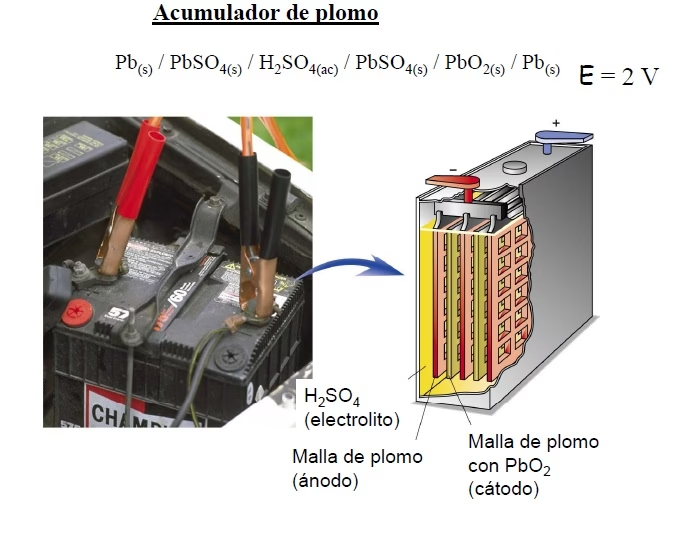
Estas baterías son conocidas por su capacidad para suministrar intensidades de corriente relativamente grandes, una característica crucial para poner en marcha motores potentes. Generalmente, proporcionan tensiones de 6 V, 12 V o múltiplos superiores, ya que cada unidad básica de energía, llamada celda, produce aproximadamente 2 V. Más allá del automóvil, este tipo de acumulador tiene una amplia gama de usos, demostrando su versatilidad y fiabilidad a lo largo del tiempo.
Historia de la Batería de Plomo-Ácido
La historia de la batería de plomo-ácido es un relato de innovación y adaptación. Fue en 1859 cuando el visionario físico e inventor francés Gaston Planté sentó las bases al desarrollar la que se considera la primera batería eléctrica recargable. Su diseño inicial era notablemente simple pero efectivo: un rollo en espiral de dos láminas de plomo puro, separadas por un tejido de lino, todo sumergido en una solución de ácido sulfúrico. Al año siguiente, Planté demostró la viabilidad de su invento presentando una batería de plomo de nueve celdas ante la Academia francesa de ciencias, acompañada de un informe técnico que destacaba su gran potencia.
El diseño de Planté fue un avance significativo, pero fue Camille Alphonse Faure quien, en 1881, lo mejoró para crear un modelo más eficiente y confiable. Esta mejora resultó ser un éxito rotundo, especialmente en los primeros automóviles eléctricos, donde la necesidad de una fuente de energía recargable y potente era primordial. La influencia de esta tecnología fue tal que, en 1899, una batería de este tipo impulsó el automóvil eléctrico 'La Jamais Contente', el primero en superar la barrera de los 100 km/h, marcando un hito en la historia del automovilismo. La batería de plomo-ácido se convirtió así en la primera batería recargable en ser comercializada a gran escala, y las baterías de automóvil modernas aún operan, en esencia, bajo los mismos principios fundamentales.
Además de su impacto en el transporte terrestre, la batería de plomo-ácido también jugó un papel crucial en la exploración submarina. Isaac Peral la eligió para propulsar su innovador submarino. Peral mejoró el diseño para hacerlo más robusto y resistente a las duras condiciones de un sumergible, asegurando su aislamiento eléctrico. Aunque las baterías debían recargarse en puerto debido a la ausencia de un sistema de recarga a bordo, proporcionaron una autonomía satisfactoria para las misiones de la época.
Constitución Física del Acumulador
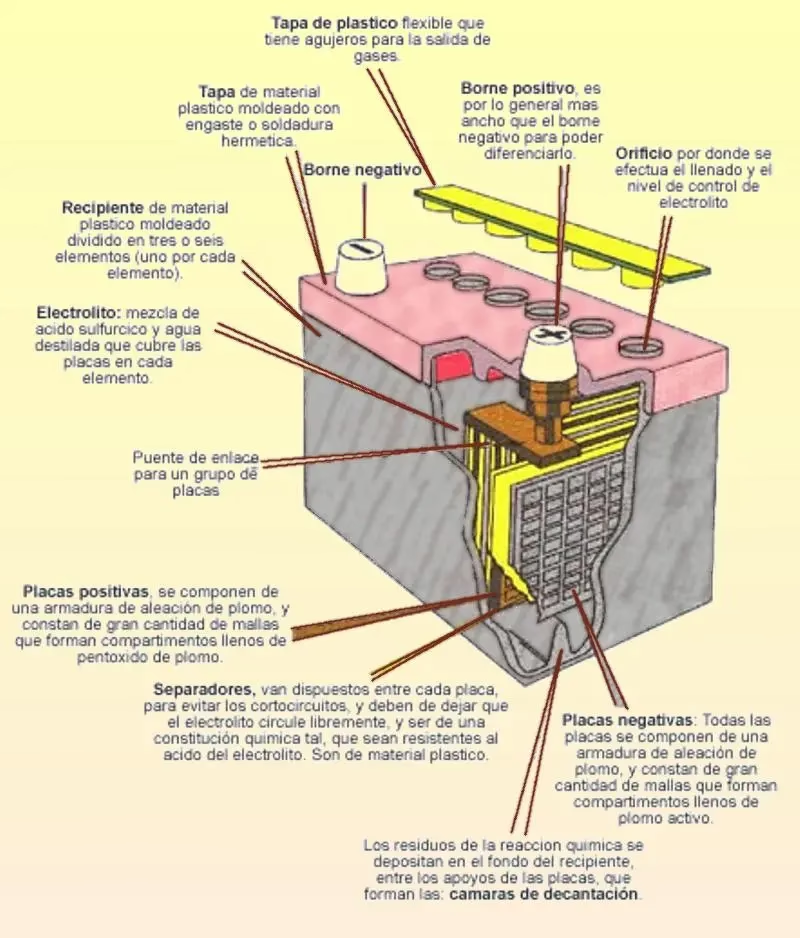
Entender cómo está construido un acumulador de plomo es clave para comprender su funcionamiento. La estructura básica consiste en un recipiente resistente que contiene una disolución de ácido sulfúrico, que actúa como el electrolito. Sumergidas en este electrolito, se encuentran un conjunto de placas de plomo dispuestas de forma paralela. Estas placas están alternadas en cuanto a su polaridad: hay placas positivas (+) y placas negativas (-).
Para garantizar la estabilidad y evitar la deformación de las placas positivas, se suele añadir una placa negativa adicional, de manera que siempre haya una placa negativa en el exterior del conjunto. En el momento de su fabricación, cuando la batería está cargada, las placas positivas suelen estar recubiertas o impregnadas de dióxido de plomo (PbO₂), mientras que las negativas están formadas por plomo esponjoso. El electrolito inicial, agregado con la batería en estado de carga completa, tiene una densidad específica, típicamente alrededor de 1,280 g/ml.
La cantidad de placas dentro de la batería influye directamente en la cantidad de corriente (intensidad) que puede suministrar; a mayor número de placas, mayor capacidad de entrega de corriente. Es importante destacar que, en la parte inferior del recipiente, se deja un espacio libre. Este espacio tiene una función práctica: permite que se depositen allí los materiales que puedan desprenderse de las placas con el tiempo, evitando que estos sedimentos causen un cortocircuito entre las placas.
Para prevenir el contacto eléctrico directo entre las placas positivas y negativas, que provocaría un cortocircuito interno, se utilizan separadores. Estos separadores son láminas hechas de material aislante que deben ser resistentes a la acción corrosiva del ácido sulfúrico y, al mismo tiempo, permitir el libre paso del electrolito y los iones entre las placas durante los procesos de carga y descarga.
En un estado de descarga, los electrodos (placas positivas y negativas) se encuentran principalmente en forma de sulfato de plomo (PbSO₄), incrustado en una matriz de plomo metálico. El electrolito, la disolución de ácido sulfúrico, cambia su densidad con el estado de carga. Con carga plena, la densidad es de aproximadamente 1,280 +/– 0,010 g/ml, y desciende hasta cerca de 1,100 g/ml cuando la batería está completamente descargada. Este cambio de densidad es un indicador útil del estado de carga de la batería.
El Proceso de Descarga: Curva y Fases
La descarga de una batería de plomo-ácido es el proceso mediante el cual la energía química almacenada se transforma en energía eléctrica que puede ser utilizada por un circuito externo. La forma en que el voltaje de la batería disminuye a medida que se descarga, bajo una carga de corriente constante, se representa típicamente mediante una curva de descarga (Voltaje vs. Tiempo). Esta curva presenta varias fases distintivas:
- Fase 1: Inicio de la Corriente de Carga (o Descarga)
Al iniciar la descarga, se produce una caída de tensión casi instantánea. Esta caída inicial está relacionada con la resistencia interna de las celdas (Ri) y la magnitud de la corriente demandada, siguiendo la Ley de Ohm. Es un descenso rápido antes de que la descarga se estabilice. - Fase 2: Curva de Tensión Constante con Carga Casi Continua
Después de la caída inicial, la tensión de la batería disminuye de manera más gradual y constante a lo largo del tiempo. Durante esta fase, la mayor parte de la energía almacenada se entrega. La pendiente de esta caída de voltaje depende de factores como el tamaño de las celdas, la química específica de la batería y la carga (corriente) que se le está demandando. Es la fase más prolongada de la descarga. - Fase 3: Caída de Tensión al Final de la Fase de Descarga
Cuando la batería se acerca a su límite de descarga, las materias primas electroquímicas (el electrolito y el material activo en las placas) se han consumido en gran medida por la reacción química. A medida que estas sustancias se agotan, la capacidad de la batería para mantener el voltaje disminuye drásticamente. La tensión cae de forma relativamente rápida. Este punto de caída rápida define el voltaje de corte o voltaje final (Us), que es el límite inferior al que se debe descargar la celda. Descargar la batería por debajo de este voltaje de corte se considera una descarga profunda o exhaustiva, lo cual somete el material activo a un estrés significativo y puede provocar una disminución permanente de la capacidad, acelerando el envejecimiento de la batería.
Procesos Químicos Internos
El funcionamiento de la batería de plomo-ácido se basa en reacciones químicas reversibles que ocurren en la interfaz entre las placas y el electrolito. Estos procesos son el corazón de su capacidad para almacenar y liberar energía.
Durante el proceso de carga, la energía eléctrica externa se utiliza para revertir las reacciones de descarga. En las placas negativas, el sulfato de plomo (PbSO₄) se reduce a plomo metálico (Pb). Simultáneamente, en las placas positivas, el sulfato de plomo se oxida para formar dióxido de plomo (PbO₂). Químicamente, esto implica una dismutación del plomo en diferentes estados de oxidación.
Un aspecto crucial durante la carga es que, bajo condiciones normales y con el voltaje de carga recomendado, no se libera hidrógeno gaseoso. Esto se debe a que la reacción de reducción de protones a hidrógeno elemental está cinéticamente inhibida en la superficie del plomo. Esta característica es muy favorable, ya que la liberación de hidrógeno podría dañar mecánicamente las placas y acortar la vida útil del acumulador. Para reforzar esta inhibición, a menudo se incorporan pequeñas cantidades de plata en los electrodos. Solo si se aplica un voltaje de carga excesivamente alto se supera este umbral, se libera hidrógeno (y oxígeno), se consume agua del electrolito y se acelera la degradación de las placas, además de crear un riesgo de explosión debido a la presencia de hidrógeno inflamable.
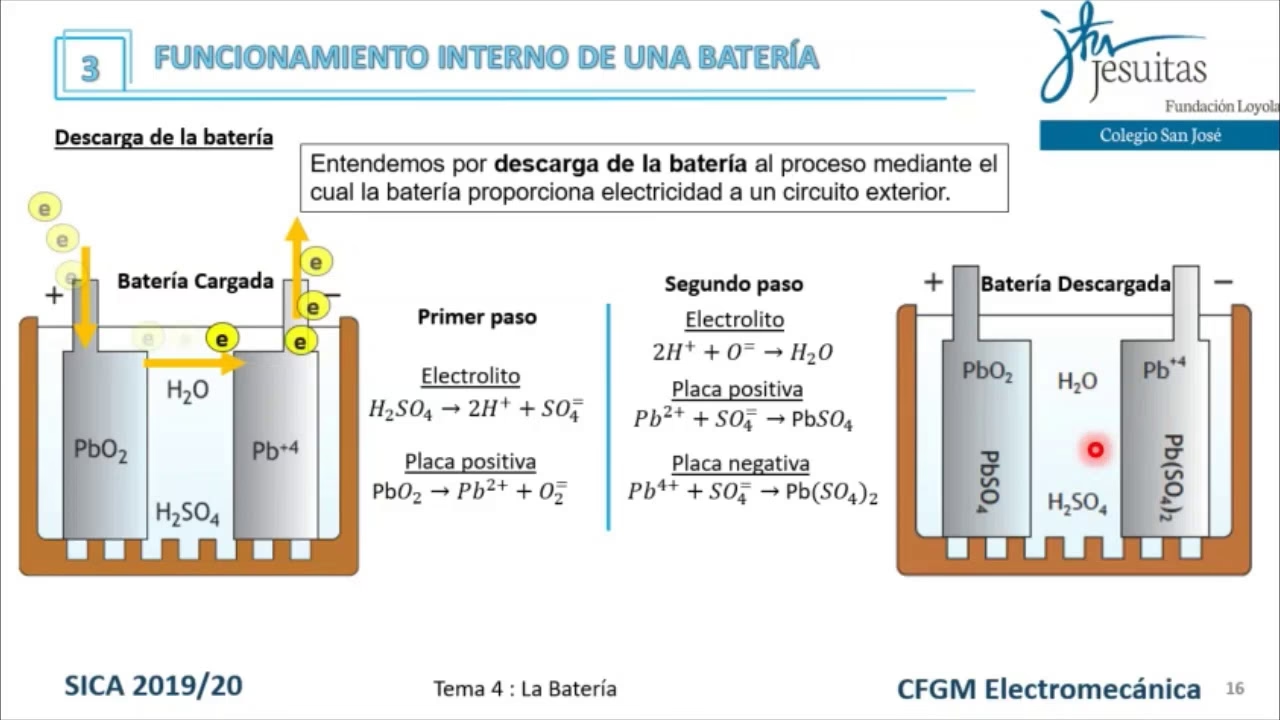
Durante la descarga, los procesos químicos se invierten. En las placas positivas, el dióxido de plomo (PbO₂) reacciona con el ácido sulfúrico para formar sulfato de plomo (PbSO₄) y agua, consumiendo electrones. En las placas negativas, el plomo metálico (Pb) reacciona con el ácido sulfúrico para formar sulfato de plomo (PbSO₄), liberando electrones. Estos electrones liberados en la placa negativa y consumidos en la positiva fluyen a través del circuito externo, generando la corriente eléctrica que utilizamos.
Las reacciones simplificadas durante la descarga son:
- En el electrodo positivo (+): PbO₂ + 2H₂SO₄ + 2e⁻ → PbSO₄ + 2H₂O + SO₄²⁻
- En el electrodo negativo (-): Pb + SO₄²⁻ → PbSO₄ + 2e⁻
La reacción global de descarga es: PbO₂ + Pb + 2H₂SO₄ → 2PbSO₄ + 2H₂O
Como se puede observar en la reacción global, durante la descarga se produce sulfato de plomo y agua, consumiendo ácido sulfúrico. Esto provoca que la concentración de ácido sulfúrico en el electrolito disminuya y, consecuentemente, su densidad también baje. Esta disminución de la densidad es un indicador fiable del estado de descarga de la batería.
La reversibilidad de estas reacciones no es perfecta e indefinida. Con el tiempo y los ciclos de carga/descarga, especialmente si la batería se descarga profundamente (por debajo de 1.8 V por celda) o se deja en estado de descarga por mucho tiempo, el sulfato de plomo puede formar cristales grandes y duros. Este fenómeno se conoce como sulfatación. El sulfato de plomo cristalizado a gran escala no reacciona eficientemente durante la carga, lo que reduce la capacidad de la batería para almacenar energía y, eventualmente, la vuelve inutilizable. En este punto, se dice que el acumulador se ha sulfatado de manera irreversible y debe ser reemplazado.
Es interesante notar que muchos acumuladores de plomo-ácido modernos utilizan un electrolito en forma de pasta o gel, en lugar de líquido. Esto mejora la seguridad al reducir el riesgo de derrames y la evaporación, haciendo su uso más cómodo.
Tensiones de Uso Típico para Baterías de 12V (6 Celdas)
El voltaje de una batería de plomo-ácido varía significativamente dependiendo de su estado de carga, la temperatura y si está bajo carga o en circuito abierto. Para una batería estándar de 12V (compuesta por 6 celdas en serie), los rangos de voltaje típicos a 20°C son los siguientes:
| Estado / Condición | Rango de Voltaje (Total) | Voltaje por Celda |
|---|---|---|
| Circuito Abierto (Inactiva) a Plena Carga | 12.6 V ~ 12.8 V | 2.10 ~ 2.13 V |
| Circuito Abierto (Inactiva) a Plena Descarga | 11.8 V ~ 12.0 V | 1.97 ~ 2.00 V |
| Bajo Carga (Demandando Corriente) a Plena Descarga | ~10.5 V | ~1.75 V |
| Carga Continua de Preservación (Flotación) - Gel | 13.4 V | ~2.23 V |
| Carga Continua de Preservación (Flotación) - AGM | 13.5 V | ~2.25 V |
| Carga Continua de Preservación (Flotación) - Electrolito Fluido | 13.8 V | ~2.30 V |
| Carga Típica (Diaria) | 14.2 V a 14.5 V | ~2.37 a ~2.42 V |
| Carga de Ecualización (Electrolito Fluido, máx. 2h) | ~15 V | ~2.50 V |
| Umbral de Gaseo | ~14.4 V | ~2.40 V |
Es crucial tener en cuenta que estos voltajes son sensibles a la temperatura. Generalmente, se requiere un ajuste de aproximadamente -0.022 V/°C por cada grado de cambio respecto a los 20°C de referencia. Las recomendaciones precisas para el voltaje de flotación son particularmente importantes para la longevidad de la batería; un voltaje demasiado bajo puede llevar a la sulfatación, mientras que un voltaje demasiado alto causa corrosión y pérdida de electrolito por gaseo. Después de completar una carga, la tensión de los terminales de la batería disminuirá rápidamente a alrededor de 13.2 V y luego descenderá más lentamente hasta estabilizarse en su voltaje de circuito abierto de plena carga, entre 12.6 V y 12.8 V.
Fallos Comunes en Baterías de Plomo-Ácido
Las baterías de plomo-ácido, especialmente las de electrolito líquido ("inundadas"), pueden experimentar diversos tipos de fallos a lo largo de su vida útil. Algunos de estos fallos son resultado del uso y mantenimiento inadecuados, mientras que otros son procesos naturales de envejecimiento. La correcta operación y el mantenimiento periódico pueden mitigar o retrasar la aparición de estos problemas, pero no los eliminan por completo.
Uno de los fallos más comunes y que limita la vida útil de la batería es la corrosión de las rejillas de los electrodos positivos. Estas rejillas, hechas de aleaciones de plomo, se oxidan gradualmente con el tiempo, transformándose en óxido de plomo. Dado que el óxido de plomo ocupa un volumen mayor que la aleación metálica original, la placa positiva "crece" o se expande. Aunque este crecimiento se considera durante el diseño de la batería, al final de su vida útil, la expansión puede ser suficiente para ejercer presión sobre la carcasa y potencialmente abrir las tapas, comprometiendo la integridad de la batería.
Otro problema frecuente es la acumulación de sedimento en el fondo del recipiente. Este sedimento está compuesto por material activo que se desprende gradualmente de las placas durante los ciclos de carga y descarga. Una cierta cantidad de sedimento es normal, pero una acumulación excesiva puede llegar a la altura de las placas y causar un cortocircuito interno entre ellas, provocando una descarga rápida o una pérdida de capacidad. Además, la presencia de sedimento puede afectar ligeramente el voltaje de flotación efectivo.
La corrosión de los conductores internos que conectan las placas a los terminales de la batería es otro punto de fallo. Este tipo de corrosión suele ocurrir cerca de la parte superior de la batería y puede quedar oculta por la tapa, dificultando su inspección visual. Aunque la batería puede parecer funcional en condiciones de baja demanda de corriente, este fallo se manifiesta dramáticamente cuando se le exige una alta intensidad, como durante el arranque del motor, momento en el que la conexión corroída no puede soportar el flujo de corriente necesario.
Preguntas Frecuentes sobre Acumuladores de Plomo
Aquí respondemos algunas preguntas comunes sobre las baterías de plomo-ácido:
¿Cómo está constituido un acumulador de plomo?
Un acumulador de plomo está compuesto principalmente por un recipiente que contiene una disolución de ácido sulfúrico (el electrolito) en la que están sumergidas placas de plomo. Estas placas se alternan en polaridad (positivas y negativas) y están separadas por materiales aislantes. Las placas positivas están recubiertas de dióxido de plomo (PbO₂) y las negativas son de plomo esponjoso cuando la batería está cargada.
¿Cómo funciona un acumulador de plomo?
Funciona mediante reacciones electroquímicas reversibles. Durante la descarga, el dióxido de plomo y el plomo reaccionan con el ácido sulfúrico para formar sulfato de plomo en ambas placas, liberando electrones que generan corriente eléctrica. Durante la carga, se aplica una corriente externa que invierte estas reacciones, reconvirtiendo el sulfato de plomo en dióxido de plomo y plomo, y restaurando la concentración de ácido sulfúrico.
¿Cómo se puede recargar un acumulador de plomo?
Un acumulador de plomo se recarga aplicando una fuente de energía eléctrica externa con un voltaje ligeramente superior al de la batería. Esta energía fuerza a que la corriente circule en sentido inverso al de la descarga, invirtiendo las reacciones químicas. El sulfato de plomo y el agua se transforman nuevamente en plomo, dióxido de plomo y ácido sulfúrico, restaurando así la carga de la batería. Es fundamental utilizar un cargador adecuado que controle el voltaje y la corriente para evitar daños.
Si quieres conocer otros artículos parecidos a Acumulador de Plomo: Constitución y Función puedes visitar la categoría Baterias.