08/12/2021
El mundo de la física está presente en muchos aspectos de nuestra vida cotidiana, a menudo sin que nos demos cuenta. Desde la forma en que caminamos hasta el funcionamiento de complejos sistemas tecnológicos, las leyes fundamentales del universo están en juego. Y sí, tu coche, esa máquina que te transporta a diario, es un verdadero laboratorio sobre ruedas donde la física se manifiesta constantemente. Hablamos de la aerodinámica, la mecánica, la termodinámica y, por supuesto, las leyes que rigen el comportamiento de los gases. Esto nos lleva a una pregunta intrigante: ¿Se aplica la Ley de Charles a los airbags, esos salvavidas inflables que pueden marcar la diferencia en un accidente?
![ESTEQUIOMETRIA de GASES | Química del AIRBAG [Cálculos Masa-Mol & Ley General]](https://i.ytimg.com/vi/PqPFZEKB3nA/hqdefault.jpg)
Para responder a esto, primero debemos entender qué postula la Ley de Charles y cómo otras leyes de los gases entran en escena cuando hablamos de sistemas automotrices.
- ¿Qué Dice la Ley de Charles Sobre los Gases?
- Un Experimento Casero que Ilustra el Principio
- Aplicaciones Clásicas de la Ley de Charles: Los Globos Aerostáticos
- La Ley de Charles y el Cero Absoluto
- Importancia General de la Ley de Charles
- ¿Se Aplica la Ley de Charles Directamente a los Airbags?
- Leyes de los Gases en Otros Sistemas del Automóvil: El Aire Acondicionado
- La Importancia de la Precisión en la Física Automotriz
- Preguntas Frecuentes
- Conclusión
¿Qué Dice la Ley de Charles Sobre los Gases?
La Ley de Charles, nombrada en honor al científico francés Jacques Charles, aunque fue Joseph Gay-Lussac quien realizó mediciones más precisas y las publicó, es una de las leyes fundamentales que describen el comportamiento de los gases ideales. Establece una relación directa entre el volumen que ocupa una cantidad fija de gas y su temperatura absoluta, siempre y cuando la presión se mantenga constante.
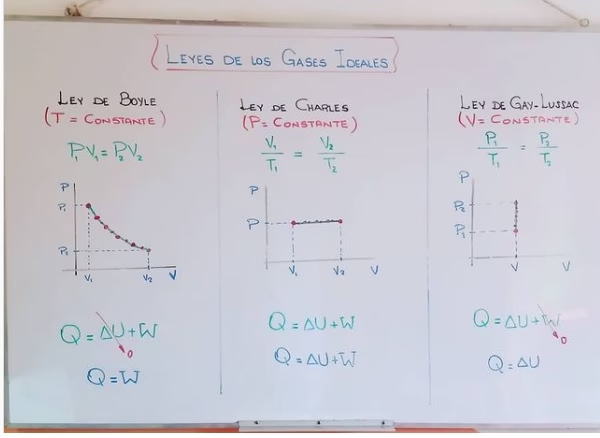
En términos sencillos, si tienes una cantidad de gas a una presión fija, aumentar su temperatura hará que se expanda y ocupe un mayor volumen. De manera inversa, disminuir la temperatura hará que se contraiga y su volumen disminuya. Matemáticamente, esto se expresa como V/T = k, donde V es el volumen, T es la temperatura absoluta (medida en Kelvin) y k es una constante para una cantidad dada de gas a presión constante.
Esta ley es intuitiva si piensas en las partículas de gas. Al calentarlas, ganan energía cinética, se mueven más rápido y chocan con más fuerza contra las paredes de su contenedor. Si el contenedor puede expandirse (para mantener la presión constante), el volumen aumentará para acomodar ese movimiento acelerado.
La Ley de Charles se aplica mejor a los gases en condiciones normales (temperaturas y presiones moderadas) y se basa en el concepto de gas ideal, un modelo teórico que simplifica el comportamiento de los gases reales.
Un Experimento Casero que Ilustra el Principio
Aunque a veces se describe de forma simplificada, el principio detrás de la Ley de Charles puede observarse en experimentos cotidianos que muestran cómo la temperatura afecta el comportamiento de los gases. Uno de ellos, aunque quizás ilustra más la relación entre temperatura y presión a volumen constante (Ley de Gay-Lussac, íntimamente relacionada y parte de las leyes de los gases), implica calentar el aire dentro de un recipiente cerrado.
Imagina frotar la parte superior de una lata de refresco. Al frotar, generas calor por fricción. Este calor se transfiere al gas (aire) contenido en el pequeño espacio de la tapa. Según los principios de las leyes de los gases, al aumentar la temperatura de un gas confinado en un volumen fijo, su presión aumenta. Si hay un punto débil, como una pequeña abertura premarcada, este aumento de presión puede ser suficiente para 'abrir' la lata desde dentro. Este experimento, aunque no es una demostración directa del cambio de volumen a presión constante como postula estrictamente la Ley de Charles, sí ilustra cómo la temperatura afecta la energía y la presión de las partículas de gas, un concepto fundamental subyacente a todas las leyes de los gases.
Aplicaciones Clásicas de la Ley de Charles: Los Globos Aerostáticos
Una de las aplicaciones más visuales y directas de la Ley de Charles es el funcionamiento de los globos aerostáticos. Desde la antigüedad, sabemos que un objeto flota en un fluido (como el aire) si es menos denso que el fluido que desplaza. La densidad es masa dividida por volumen.
Un globo aerostático funciona calentando el aire dentro de la envoltura. Según la Ley de Charles, al aumentar la temperatura del aire dentro del globo (manteniendo la presión aproximadamente igual a la del aire exterior, ya que el globo está abierto en la parte inferior), su volumen se expande. Sin embargo, la cantidad de masa de aire dentro del globo disminuye (parte del aire caliente escapa por la abertura). Pero el efecto principal es que el aire caliente dentro del globo se vuelve significativamente menos denso que el aire frío y más denso del exterior.

Como el volumen total del globo es grande y está lleno de aire menos denso, el peso total del aire caliente dentro del globo y la estructura del globo es menor que el peso del volumen equivalente de aire frío exterior que desplaza. Esta diferencia de peso genera una fuerza de flotación hacia arriba, permitiendo que el globo se eleve. Es un ejemplo perfecto de cómo el aumento de temperatura lleva a una disminución de densidad (por el aumento de volumen o escape de masa), generando flotación.
La Ley de Charles y el Cero Absoluto
Si extrapolamos la relación lineal entre volumen y temperatura descrita por la Ley de Charles, teóricamente llegamos a una temperatura en la que el volumen de un gas ideal sería cero. Esta temperatura es el cero absoluto, equivalente a -273.15 grados Celsius o 0 Kelvin. Sin embargo, es importante notar que los gases reales no se comportan como gases ideales a temperaturas muy bajas. Antes de alcanzar el cero absoluto, los gases reales se licúan o solidifican, por lo que la Ley de Charles deja de ser aplicable en la práctica a temperaturas extremadamente bajas.
Importancia General de la Ley de Charles
La Ley de Charles, junto con las leyes de Boyle (presión y volumen a temperatura constante) y Gay-Lussac (presión y temperatura a volumen constante), es fundamental para comprender el comportamiento de los gases. Estas leyes tienen aplicaciones cruciales en diversos campos, desde la meteorología hasta la química industrial, pasando por el transporte y almacenamiento de gases.
¿Se Aplica la Ley de Charles Directamente a los Airbags?
Ahora volvamos a la pregunta central: ¿Rige la Ley de Charles el funcionamiento de los airbags? La respuesta corta es: no directamente como la única ley aplicable, y no en el sentido estricto de un proceso a presión constante.
Los airbags son sistemas de seguridad diseñados para inflarse en milisegundos durante una colisión. Esto se logra mediante una reacción química muy rápida que genera una gran cantidad de gas, típicamente nitrógeno (N₂). Este gas llena una bolsa de tela plegada, creando un cojín para proteger a los ocupantes del vehículo.
Durante la inflación de un airbag, ocurren varios cambios simultáneamente:
- Se genera una gran cantidad de gas (n).
- El volumen del airbag aumenta drásticamente de casi cero a su tamaño completo.
- La temperatura del gas aumenta debido a la naturaleza exotérmica de la reacción química.
- La presión dentro del airbag aumenta significativamente para inflarlo y mantener su rigidez momentánea.
Como puedes ver, en el proceso de inflado de un airbag, ni la presión, ni el volumen, ni la temperatura, ni la cantidad de gas permanecen constantes. Por lo tanto, una ley que solo relaciona dos variables (como la Ley de Charles, que relaciona volumen y temperatura a presión constante) no es suficiente para describir completamente este proceso dinámico.
La ley que mejor aproxima el comportamiento de los gases en un sistema como un airbag es la Ley de los Gases Ideales, cuya fórmula es PV = nRT. Esta ley relaciona la presión (P), el volumen (V), la cantidad de sustancia (n, en moles), la temperatura absoluta (T) y la constante de los gases ideales (R).

La Ley de los Gases Ideales es una combinación de las leyes de Boyle, Charles y Avogadro (que relaciona volumen y cantidad de gas a temperatura y presión constantes) y, en cierta medida, incorpora la relación de Gay-Lussac. Para los ingenieros que diseñan airbags, la Ley de los Gases Ideales proporciona un modelo mucho más útil para calcular la cantidad precisa de propelente químico necesaria (para obtener el 'n' correcto) y predecir la presión y el volumen resultantes a la temperatura generada, asegurando que el airbag se infle al tamaño y rigidez adecuados en el momento justo para una máxima protección.
Si bien la Ley de Charles por sí sola no rige el inflado de un airbag, el principio de que un aumento de temperatura tiende a aumentar el volumen o la presión de un gas (dependiendo de las restricciones) es fundamental y forma parte de la comprensión más amplia que lleva a la Ley de los Gases Ideales. La rápida generación de gas caliente es precisamente lo que permite que el airbag se infle tan velozmente.
Leyes de los Gases en Otros Sistemas del Automóvil: El Aire Acondicionado
Aunque la Ley de Charles no sea la protagonista en la explicación de los airbags, las leyes de los gases, incluida la de Charles, son cruciales en otros sistemas automotrices. Un excelente ejemplo es el sistema de aire acondicionado.
Los sistemas de aire acondicionado de los coches utilizan un refrigerante que cambia de estado (entre líquido y gas) y circula por un circuito cerrado. El funcionamiento se basa en la manipulación de la presión y la temperatura del refrigerante, un proceso que se describe mediante la Ley Combinada de los Gases (PV/T = k), que, como su nombre indica, combina las leyes de Boyle, Charles y Gay-Lussac.
El ciclo básico es el siguiente:
- El compresor (ubicado en la unidad exterior, bajo el capó) aumenta la presión del refrigerante gaseoso. Según la Ley Combinada (o más específicamente, la relación presión-temperatura a volumen cambiante), aumentar la presión también aumenta su temperatura.
- El refrigerante caliente a alta presión fluye hacia el condensador (generalmente en la parte delantera del coche, cerca del radiador), donde disipa el calor al aire exterior (ayudado por un ventilador). Al enfriarse a alta presión, el refrigerante se condensa y se convierte en líquido.
- El refrigerante líquido a alta presión pasa por un dispositivo de medición o válvula de expansión, que restringe el flujo y provoca una caída drástica de la presión. Según la Ley Combinada, disminuir la presión de un gas o líquido (en este caso, pasando a través de una restricción) provoca una caída de temperatura. El refrigerante se enfría considerablemente.
- El refrigerante frío a baja presión entra en el evaporador (ubicado dentro del salpicadero, en la unidad interior). El aire caliente del habitáculo es soplado a través de las aletas frías del evaporador. El calor del aire es absorbido por el refrigerante, haciendo que este se evapore y vuelva a convertirse en gas. Este proceso de absorción de calor enfría el aire que luego se impulsa hacia el habitáculo.
- El refrigerante gaseoso caliente a baja presión regresa al compresor para comenzar el ciclo de nuevo.
En este ciclo, la relación entre presión y temperatura (Gay-Lussac), volumen y temperatura (Charles), y presión y volumen (Boyle) son fundamentales para que el refrigerante cambie de estado y transfiera calor eficazmente. Así, aunque no sea en los airbags, la Ley de Charles y las leyes de los gases derivadas de ella son absolutamente esenciales para el confort térmico en tu coche.
La Importancia de la Precisión en la Física Automotriz
La aplicación correcta de las leyes de los gases, ya sea la Ley de los Gases Ideales para los airbags o la Ley Combinada para el aire acondicionado, subraya la importancia de la precisión en la ingeniería automotriz. Un cálculo incorrecto en la cantidad de gas generador para un airbag podría resultar en un inflado insuficiente (poca protección) o excesivo (riesgo de lesiones por el propio airbag). De manera similar, un sistema de aire acondicionado mal diseñado basado en una comprensión imperfecta de las leyes de los gases sería ineficiente o incapaz de enfriar adecuadamente.
Preguntas Frecuentes
Aclaramos algunas dudas comunes:
¿Qué gas se utiliza típicamente para inflar un airbag?
El gas más común utilizado es el nitrógeno (N₂), generado por la descomposición rápida de compuestos químicos como la azida de sodio (NaN₃) en una reacción controlada.

¿Qué ley de la física describe mejor el funcionamiento de un airbag?
La Ley de los Gases Ideales (PV = nRT) es la que mejor describe el comportamiento del gas dentro de un airbag durante su inflación, ya que considera los cambios simultáneos en presión, volumen, temperatura y la cantidad de gas.
¿Por qué la Ley de Charles no es suficiente para explicar un airbag?
La Ley de Charles describe la relación entre volumen y temperatura solo cuando la presión es constante. En un airbag, la presión aumenta drásticamente durante el inflado, por lo que la Ley de Charles por sí sola no puede modelar el proceso completo.
¿Se aplican las leyes de los gases en otros componentes del automóvil?
Sí, las leyes de los gases son fundamentales para el funcionamiento de sistemas como el aire acondicionado, donde se manipulan la presión y la temperatura de un refrigerante.
¿Es la temperatura importante en el diseño de airbags?
Absolutamente. La reacción química que genera el gas es exotérmica (produce calor), lo que aumenta la temperatura del gas. Los ingenieros deben tener en cuenta esta temperatura elevada al diseñar el airbag y el sistema de ventilación para asegurar un inflado seguro y eficaz, y para evitar quemaduras por contacto con el gas caliente o la bolsa.
¿Qué es el cero absoluto según la Ley de Charles?
Es la temperatura teórica (-273.15 °C o 0 K) a la que, según la extrapolación de la Ley de Charles para un gas ideal a presión constante, el volumen del gas sería cero. En la práctica, los gases reales cambian de estado antes de alcanzar esta temperatura.
Conclusión
En resumen, aunque la Ley de Charles postula una relación fundamental entre el volumen y la temperatura de un gas a presión constante y es crucial para entender fenómenos como los globos aerostáticos y sistemas como el aire acondicionado automotriz, no es la ley principal que describe el complejo y rápido proceso de inflado de un airbag. Para los airbags, donde la presión, el volumen, la temperatura y la cantidad de gas cambian simultáneamente, la Ley de los Gases Ideales (PV=nRT) proporciona un modelo mucho más preciso y útil para el diseño y la ingeniería de estos sistemas de seguridad vitales. La física, en sus diversas formas, es una parte integral e indispensable de la tecnología que hace que nuestros vehículos sean más seguros y confortables.
Si quieres conocer otros artículos parecidos a Leyes de Gases: ¿Airbags y Ley de Charles? puedes visitar la categoría Automóviles.

