15/09/2023
Las baterías son omnipresentes en el mundo moderno. Dependemos de estas fuentes de energía portátiles para alimentar una vasta gama de dispositivos, desde nuestros teléfonos móviles y audífonos hasta, crucialmente, nuestros automóviles. A pesar de su prevalencia en la vida cotidiana, el funcionamiento interno de una batería a menudo pasa desapercibido. ¿Sabes realmente cómo funciona una batería? ¿Podrías explicar la ciencia detrás de la chispa que enciende tu motor?

La magia que permite a una batería almacenar y liberar energía radica en un proceso químico fundamental conocido como reacción de oxidación-reducción, o redox. Esta intrincada danza de electrones e iones es lo que convierte la energía química almacenada en energía eléctrica utilizable, impulsando todo, desde una simple linterna hasta los complejos sistemas de un vehículo.
- Anatomía de una Batería: Los Componentes Clave
- La Ciencia Detrás de la Potencia: Reacciones Electroquímicas
- Redox: El Corazón Químico de la Batería
- Cómo Funciona una Batería: El Ciclo de Descarga
- Baterías Recargables vs. No Recargables
- La Reacción Redox en una Batería de Automóvil
- Terminología Clave sobre Baterías
- Preguntas Frecuentes (FAQs)
- Conclusión
Anatomía de una Batería: Los Componentes Clave
Para entender cómo funciona una batería a nivel químico, primero debemos conocer sus partes esenciales. La mayoría de las baterías básicas constan de tres componentes principales:
- Electrodos: Hay dos electrodos en cada batería. Ambos están hechos de materiales conductores, pero desempeñan roles distintos.
- Electrolito: Esta es una sustancia, a menudo líquida o gelatinosa, que contiene partículas cargadas eléctricamente llamadas iones. Se encuentra entre los electrodos y también dentro de ellos.
- Separador: Este componente tiene una función sencilla pero vital: mantener los dos electrodos separados físicamente dentro de la batería.
Los dos electrodos tienen nombres específicos según su función durante la descarga de la batería (cuando está suministrando energía). El electrodo conectado al terminal positivo de la batería se conoce como cátodo. Es el lugar donde la corriente eléctrica sale (o los electrones entran) durante la descarga. El otro electrodo, conectado al terminal negativo, es el ánodo. Aquí es donde la corriente eléctrica entra (o los electrones salen) durante la descarga.
El electrolito es crucial porque permite el movimiento de los iones entre los electrodos. Estos iones interactúan con los materiales de los electrodos, produciendo las reacciones químicas necesarias para generar una corriente eléctrica. Sin el separador, los electrodos entrarían en contacto directo, provocando un cortocircuito que impediría el correcto funcionamiento de la batería.
La Ciencia Detrás de la Potencia: Reacciones Electroquímicas
En esencia, una batería funciona gracias a una serie de reacciones químicas que tienen lugar en sus electrodos y en el electrolito. Cuando conectas una batería a un circuito (como encender una linterna o arrancar un coche), estás completando un camino para que la energía fluya. La energía química almacenada dentro de la batería se transforma en energía eléctrica.
Las interacciones entre los iones del electrolito y los átomos de los materiales de los electrodos dan lugar a lo que se conocen como reacciones electroquímicas. Estas reacciones son la fuente de la corriente eléctrica que la batería proporciona.
Redox: El Corazón Químico de la Batería
El conjunto de reacciones químicas que ocurren en los electrodos de una batería se conoce colectivamente como reacciones de oxidación-reducción, o redox. Este nombre deriva de los dos procesos que ocurren simultáneamente:
- Oxidación: Ocurre en el ánodo. Es el proceso por el cual un material pierde electrones. Se dice que el ánodo es el agente reductor, ya que causa la reducción en el otro electrodo al cederle electrones.
- Reducción: Ocurre en el cátodo. Es el proceso por el cual un material gana electrones. Se dice que el cátodo es el agente oxidante, ya que causa la oxidación en el ánodo al aceptar sus electrones.
En una batería, estas reacciones redox resultan en el flujo de iones a través del electrolito entre el ánodo y el cátodo, y, crucialmente, en la liberación de electrones de los átomos del electrodo. Estos electrones libres se acumulan en el ánodo (el terminal negativo).

Como resultado de la liberación y consumo de electrones, los dos electrodos desarrollan cargas diferentes. El ánodo se vuelve negativamente cargado a medida que libera electrones, mientras que el cátodo se vuelve positivamente cargado a medida que consume electrones (que tienen carga negativa). Esta diferencia de carga crea una 'presión' eléctrica (voltaje) que impulsa a los electrones a moverse hacia el cátodo cargado positivamente. Sin embargo, dentro de la batería, el separador impide que los electrones se muevan directamente del ánodo al cátodo.
Cómo Funciona una Batería: El Ciclo de Descarga
Consideremos el ejemplo de una linterna con pilas alcalinas AA. Cuando insertas las pilas y enciendes la linterna, completas el circuito eléctrico. Los electrones acumulados en el ánodo de la pila ahora tienen un camino externo (a través del circuito de la linterna) para llegar al cátodo. Este flujo de electrones a través del circuito externo es lo que constituye la corriente eléctrica que alimenta la bombilla de la linterna.
La energía química almacenada en la pila se convierte en energía eléctrica, que viaja fuera de la pila (desde el ánodo negativo), pasa por la bombilla (haciéndola brillar) y regresa a la pila por el otro extremo (el cátodo positivo). Dentro de la pila, las reacciones redox continúan, manteniendo el flujo de electrones a través del circuito externo y el flujo de iones a través del electrolito interno, hasta que los materiales activos se agotan o se transforman.
Baterías Recargables vs. No Recargables
El proceso redox es fundamental en ambos tipos de baterías, pero con una diferencia clave:
- Baterías primarias (no recargables): En estas baterías, como las pilas alcalinas comunes, las reacciones químicas que generan energía eventualmente se detienen de forma irreversible. Una vez que los materiales activos se han consumido, la batería está 'agotada' y no puede generar más corriente. Los procesos electroquímicos no pueden invertirse fácilmente.
- Baterías secundarias (recargables): En estas baterías, como las de iones de litio, níquel-cadmio, níquel-metal hidruro o las de plomo-ácido (comunes en automóviles), las reacciones electroquímicas pueden revertirse. Al aplicar una fuente de energía eléctrica externa (como un cargador), se fuerza a los electrones a fluir en la dirección opuesta, revirtiendo las reacciones redox y restaurando los materiales activos a su estado original, permitiendo que la batería vuelva a almacenar energía química para futuras descargas.
La Reacción Redox en una Batería de Automóvil
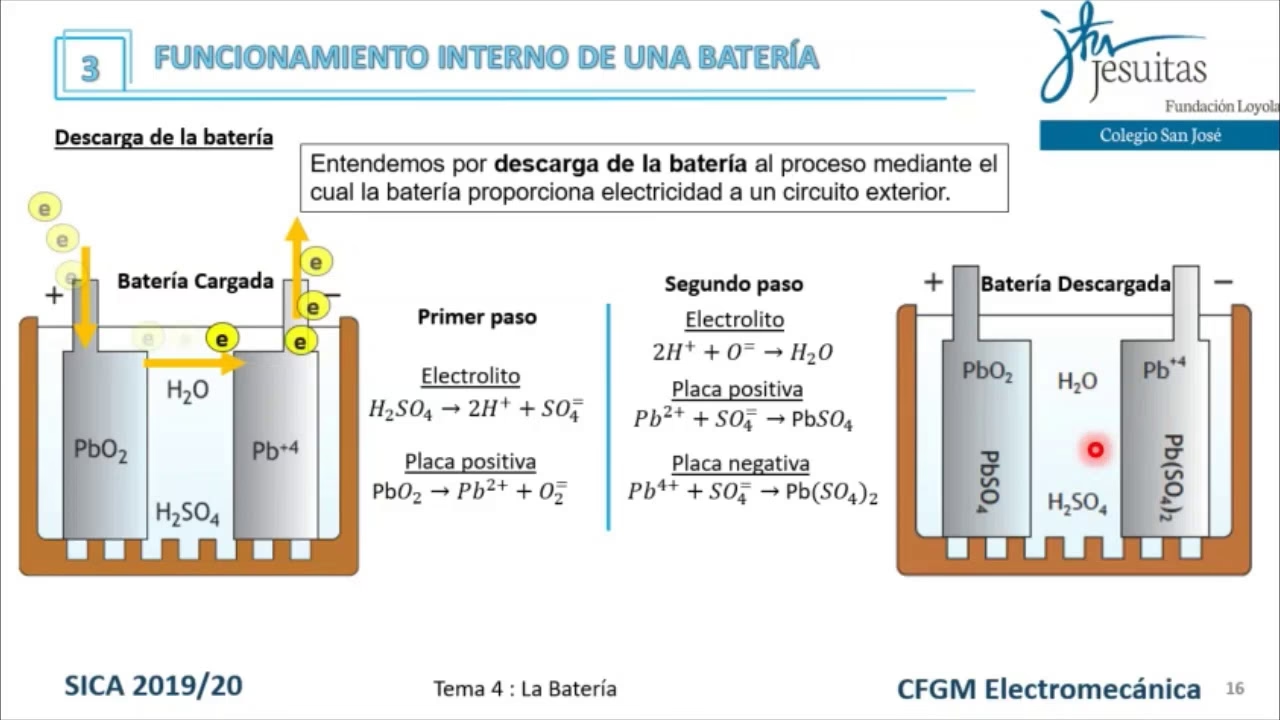
Las baterías de automóvil más comunes, especialmente en vehículos no eléctricos, son las baterías de plomo-ácido. Estas baterías operan bajo el mismo principio general de las reacciones redox descrito anteriormente.
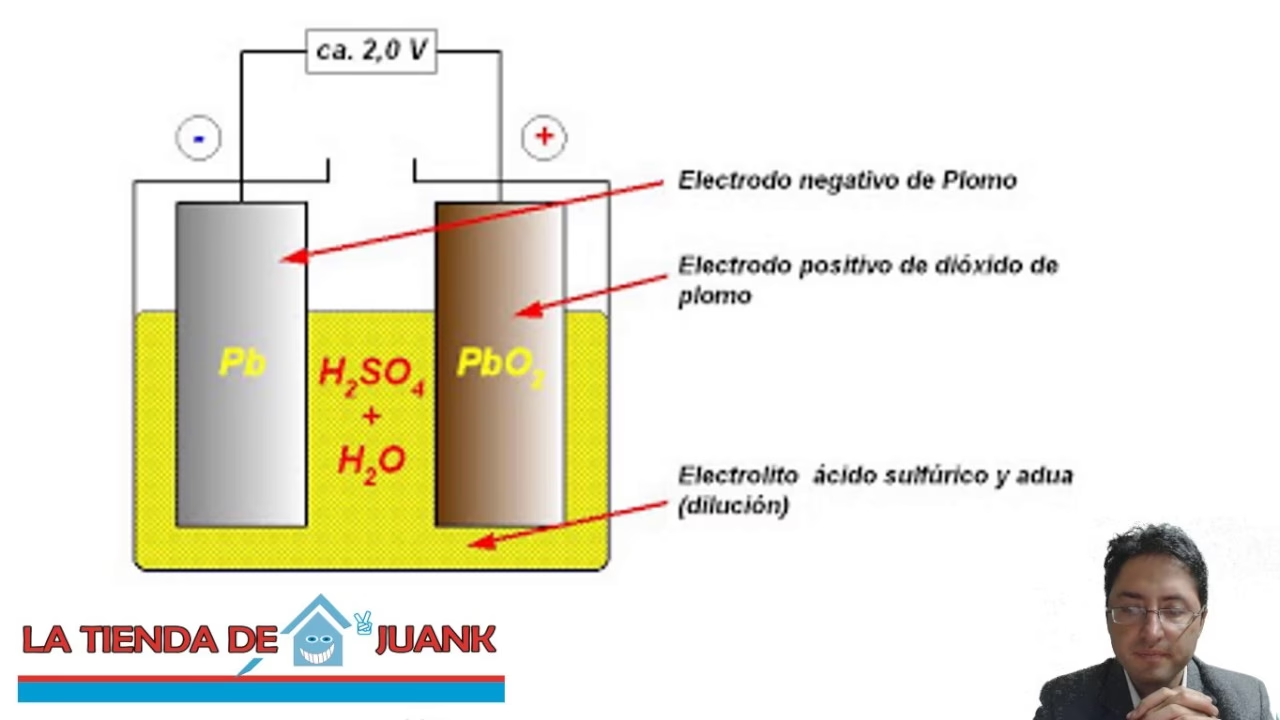
Una batería de plomo-ácido típica de automóvil tiene un voltaje nominal de 12 voltios. Esto se logra conectando en serie seis celdas individuales, cada una con un voltaje de aproximadamente 2.0 voltios. Cada una de estas celdas contiene electrodos hechos principalmente de plomo y óxido de plomo, sumergidos en un electrolito de ácido sulfúrico diluido.

Durante la descarga (por ejemplo, al arrancar el motor), ocurren reacciones redox en el ánodo (plomo) y el cátodo (óxido de plomo), facilitadas por el electrolito. Estas reacciones liberan electrones que fluyen a través del circuito externo para alimentar el motor de arranque y otros sistemas eléctricos. Simultáneamente, los iones se mueven a través del electrolito para mantener la neutralidad de carga en los electrodos.
Aunque no se detallan las reacciones químicas específicas aquí (ya que la información proporcionada no las incluye), el principio subyacente es el mismo: una sustancia se oxida (pierde electrones) en el ánodo, mientras que otra sustancia se reduce (gana electrones) en el cátodo. Este intercambio de electrones, impulsado por las diferencias de potencial químico, genera la corriente eléctrica que pone en marcha el vehículo.
Cuando el alternador del automóvil está funcionando o cuando la batería se conecta a un cargador externo, el proceso se invierte. Se aplica una energía eléctrica externa que fuerza a las reacciones redox a ocurrir en la dirección opuesta, reconvirtiendo los productos de la descarga en los materiales originales de plomo y óxido de plomo, recargando así la batería.
Terminología Clave sobre Baterías
Comprender algunos términos técnicos ayuda a hablar sobre el rendimiento y las características de las baterías:
| Término | Descripción |
|---|---|
| Voltaje | También conocido como voltaje nominal de celda, describe la "presión" eléctrica con la que los electrones libres se mueven a través del circuito. Mayor voltaje significa mayor fuerza eléctrica. Una celda de plomo-ácido típica tiene 2V, y una batería de coche de 12V tiene seis de estas celdas en serie. |
| Amperios (Amps) | Una medida de la corriente eléctrica, es decir, la cantidad de electrones que fluyen a través de un circuito en un período de tiempo determinado. |
| Capacidad | Medida en amperios-hora (Ah). Indica cuánta carga total puede suministrar una batería. Por ejemplo, una batería de 1 Ah puede suministrar una corriente de 1 amperio durante 1 hora (o 0.5 A durante 2 horas, etc.) antes de que su voltaje caiga por debajo de un umbral utilizable. |
| Densidad de Potencia | Describe la cantidad de potencia que una batería puede entregar por unidad de peso. Es importante para aplicaciones que requieren ráfagas rápidas de energía, como la aceleración de un vehículo eléctrico. |
| Densidad de Energía | Describe cuánta energía total puede almacenar una batería por unidad de volumen o masa. Este valor impacta directamente en cuánto tiempo puede funcionar un dispositivo (ej. duración de la batería del teléfono) o cuán lejos puede viajar un vehículo eléctrico con una sola carga. |
Estos términos nos permiten comparar y seleccionar baterías según la aplicación específica, entendiendo las capacidades que ofrecen más allá de simplemente "funciona".
Preguntas Frecuentes (FAQs)
¿Qué es una pila redox?
Una pila o batería redox es un dispositivo electroquímico que convierte energía química en energía eléctrica (y viceversa en el caso de las recargables) mediante reacciones de oxidación-reducción. Las "baterías de flujo redox" mencionadas en parte de la información se refieren a un tipo específico de batería donde los materiales activos (electrolitos) se almacenan externamente y se bombean a través de una celda electroquímica donde ocurren las reacciones redox. Sin embargo, el principio redox aplica a la mayoría de las baterías, incluidas las de coche.

¿Cómo funciona una batería redox?
Una batería redox funciona facilitando el movimiento de electrones desde un material que se oxida (ánodo) hacia un material que se reduce (cátodo) a través de un circuito externo, generando así una corriente eléctrica. Internamente, los iones se mueven a través del electrolito para equilibrar las cargas. Este proceso es impulsado por las reacciones químicas redox que convierten la energía química almacenada en energía eléctrica.
¿Cómo funciona el redox de una batería?
El funcionamiento redox de una batería se basa en la transferencia de electrones. En el ánodo (terminal negativo durante la descarga), ocurre la oxidación (pérdida de electrones). En el cátodo (terminal positivo durante la descarga), ocurre la reducción (ganancia de electrones). Los electrones liberados en el ánodo viajan a través del circuito externo hacia el cátodo, constituyendo la corriente eléctrica. Este ciclo de oxidación y reducción es la esencia del proceso redox que permite a la batería generar electricidad.
¿Cuál es la reacción redox en una batería de automóvil?
En una batería de automóvil de plomo-ácido, la reacción redox implica la oxidación del plomo en el ánodo y la reducción del óxido de plomo en el cátodo, en presencia de ácido sulfúrico como electrolito, durante la descarga. Aunque las ecuaciones químicas específicas son complejas y no se detallan en la información proporcionada, el principio fundamental es que la transferencia de electrones entre los compuestos de plomo, mediada por el electrolito, es la reacción redox que genera la electricidad necesaria para alimentar el vehículo. Durante la recarga, el proceso se invierte.
Conclusión
La capacidad de un automóvil para arrancar y alimentar sus sistemas eléctricos depende fundamentalmente de las reacciones de oxidación-reducción que ocurren dentro de su batería. Este proceso redox, que implica la transferencia controlada de electrones entre diferentes materiales, es la base de cómo la energía química se convierte eficientemente en la energía eléctrica que necesitamos. Comprender esta ciencia básica no solo desmitifica un componente esencial de nuestros vehículos, sino que también resalta la ingeniosidad de los sistemas electroquímicos que impulsan gran parte de nuestra tecnología moderna.
Si quieres conocer otros artículos parecidos a La Química que Impulsa tu Auto: Redox en Baterías puedes visitar la categoría Automóviles.