12/05/2022
En el vasto universo de la química, existen procesos fundamentales que rigen innumerables fenómenos a nuestro alrededor. Entre ellos, las reacciones de oxidación-reducción, comúnmente conocidas como reacciones redox, ocupan un lugar central. Estas reacciones son aquellas en las que los átomos de las sustancias involucradas experimentan un cambio en su estado de oxidación. Este cambio se produce debido a la transferencia de electrones entre las especies químicas reaccionantes. Es crucial entender que la oxidación y la reducción son procesos que ocurren siempre de forma simultánea: si una sustancia se oxida (pierde electrones), otra sustancia debe reducirse (ganar esos electrones).

Las reacciones redox se describen a menudo mediante el uso de semiecuaciones, que representan por separado los procesos de donación y aceptación de electrones. Su importancia trasciende los laboratorios y se manifiesta en una gran variedad de procesos naturales y tecnológicos, desde la respiración celular y la fotosíntesis, que sustentan la vida, hasta la corrosión de los metales y la generación de energía en baterías. Pero uno de los roles más impactantes de las reacciones redox, especialmente relevante en el contexto de los automóviles y la industria, es su participación esencial en la combustión de combustibles.
- Conceptos Fundamentales de las Reacciones Redox
- ¿Cómo Ocurren las Reacciones Redox?
- Reacciones Redox en la Vida Diaria
- La Combustión de Combustibles: Una Reacción Redox Clave
- Otros Ejemplos Orgánicos y Bioquímicos
- Tabla Resumen de Conceptos Clave
- Preguntas Frecuentes sobre Reacciones Redox y Combustión
- ¿Por qué la oxidación y la reducción siempre ocurren juntas?
- ¿Qué significa el estado de oxidación?
- ¿El oxígeno es siempre el agente oxidante en una reacción redox?
- ¿Cómo se identifica si un compuesto orgánico se oxida o se reduce?
- ¿Todas las reacciones que producen energía son redox?
- ¿Qué relación tienen las reacciones redox con la corrosión de los autos?
- ¿La energía de la combustión proviene directamente de la transferencia de electrones?
Conceptos Fundamentales de las Reacciones Redox
Para comprender a fondo las reacciones redox, es necesario familiarizarse con algunos términos clave:
Estado de Oxidación
El estado de oxidación es un concepto formal que representa la carga hipotética que un átomo tendría si todos los enlaces químicos en un compuesto fueran completamente iónicos. Aunque en la realidad los enlaces pueden ser covalentes, este concepto es una herramienta fundamental para rastrear el movimiento aparente de electrones en una reacción. Se indica con un número (positivo, negativo o cero) generalmente en números romanos. Los elementos en diferentes estados de oxidación exhiben distintas propiedades redox.
Oxidación
La oxidación es el proceso en el cual una sustancia pierde electrones, lo que resulta en un aumento de su estado de oxidación. La sustancia que se oxida actúa como agente reductor, ya que provoca la reducción de otra sustancia al cederle electrones. La oxidación nunca ocurre sola; siempre va acompañada de la reducción de otra especie.
Reducción
La reducción es el proceso opuesto a la oxidación. Implica la ganancia de electrones por parte de una sustancia, lo que lleva a una disminución de su estado de oxidación. La sustancia que se reduce actúa como agente oxidante, ya que provoca la oxidación de otra sustancia al aceptar sus electrones. Como se mencionó, la reducción y la oxidación son interdependientes.
Reacción de Desproporción (Dismutación)
Este es un tipo particular de reacción redox donde un mismo elemento se oxida y se reduce simultáneamente. Para que esto ocurra, el elemento debe poder existir en al menos tres estados de oxidación diferentes, siendo el estado intermedio inestable y tendiendo a convertirse en los otros dos. Átomos como el azufre, nitrógeno, fósforo o manganeso pueden experimentar este tipo de reacción.
Reacción de Sinproporción
También conocida como dismutación inversa, la sinproporción ocurre cuando dos compuestos diferentes que contienen el mismo elemento en distintos estados de oxidación reaccionan para formar un producto donde ese elemento se encuentra en un nuevo estado de oxidación, generalmente intermedio a los estados iniciales.
Equilibrio Electrónico
En cualquier reacción redox completa, la cantidad total de electrones perdidos por la especie que se oxida debe ser igual a la cantidad total de electrones ganados por la especie que se reduce. Este principio se conoce como equilibrio electrónico y es fundamental para ajustar (balancear) las ecuaciones redox.
¿Cómo Ocurren las Reacciones Redox?
El mecanismo central de una reacción redox es la transferencia de electrones. Para representar y comprender estas reacciones, se utilizan las semiecuaciones de oxidación y reducción. Por ejemplo, si el sodio metálico (estado de oxidación 0) reacciona con cloro gaseoso (estado de oxidación 0) para formar cloruro de sodio (Na+ Cl-, donde Na tiene estado +1 y Cl tiene estado -1):
- Semiecuación de oxidación: Na → Na+ + e- (el sodio pierde un electrón y su estado de oxidación aumenta de 0 a +1)
- Semiecuación de reducción: Cl2 + 2e- → 2Cl- (el cloro gana electrones y su estado de oxidación disminuye de 0 a -1)
Para obtener la ecuación global balanceada, se ajusta el número de electrones perdidos y ganados. En este caso, se necesitan dos átomos de sodio para donar dos electrones, que son aceptados por una molécula de Cl2:
- 2Na → 2Na+ + 2e-
- Cl2 + 2e- → 2Cl-
Sumando ambas semiecuaciones se obtiene la reacción redox completa: 2Na + Cl2 → 2NaCl. El sodio es el reductor y el cloro es el oxidante.
Los agentes oxidantes más comunes suelen ser elementos con alta electronegatividad (como el oxígeno y los halógenos), iones metálicos en altos estados de oxidación, iones de metales nobles y ácidos oxidantes fuertes (como el ácido nítrico o el sulfúrico concentrado). Algunos ejemplos incluyen KMnO4, K2Cr2O7 o H2O2. Los agentes reductores típicos son elementos electropositivos (metales alcalinos y alcalinotérreos), metales en estado de oxidación cero, hidrógeno molecular (H2), carbono (C), monóxido de carbono (CO) y aniones de ciertos ácidos inorgánicos (como Cl-, Br-, SCN-). Ejemplos comunes son Na, Mg, Fe2+ o H2.
La fuerza impulsora de una reacción redox está relacionada con el potencial redox de las especies involucradas. Cuanto mayor sea la diferencia de potencial entre el oxidante y el reductor, mayor será la tendencia a que la reacción ocurra.
Reacciones Redox en la Vida Diaria
Lejos de ser conceptos puramente académicos, las reacciones redox son omnipresentes en nuestra vida cotidiana y en el funcionamiento de la naturaleza:
- Fotosíntesis: Las plantas utilizan la energía solar para convertir dióxido de carbono y agua en glucosa (un azúcar) y oxígeno. El agua se oxida y el dióxido de carbono se reduce.
- Respiración Celular: Las células obtienen energía oxidando glucosa (u otros nutrientes) con oxígeno, produciendo dióxido de carbono, agua y ATP (la molécula de energía celular). La glucosa se oxida y el oxígeno se reduce.
- Corrosión: La oxidación de metales, como la formación de óxido en el hierro, es un proceso redox donde el metal se oxida y el oxígeno (u otros agentes) se reduce.
- Baterías: Las pilas y baterías generan electricidad a través de reacciones redox espontáneas. La descarga implica la oxidación de un material en un electrodo y la reducción de otro en el otro electrodo. La recarga invierte el proceso.
- Blanqueo: Muchos agentes blanqueadores funcionan oxidando los cromóforos (moléculas que dan color) en las manchas.
- Antioxidantes: Sustancias como la Vitamina C y E son antioxidantes; actúan como agentes reductores, protegiendo a las células de la oxidación dañina causada por radicales libres.
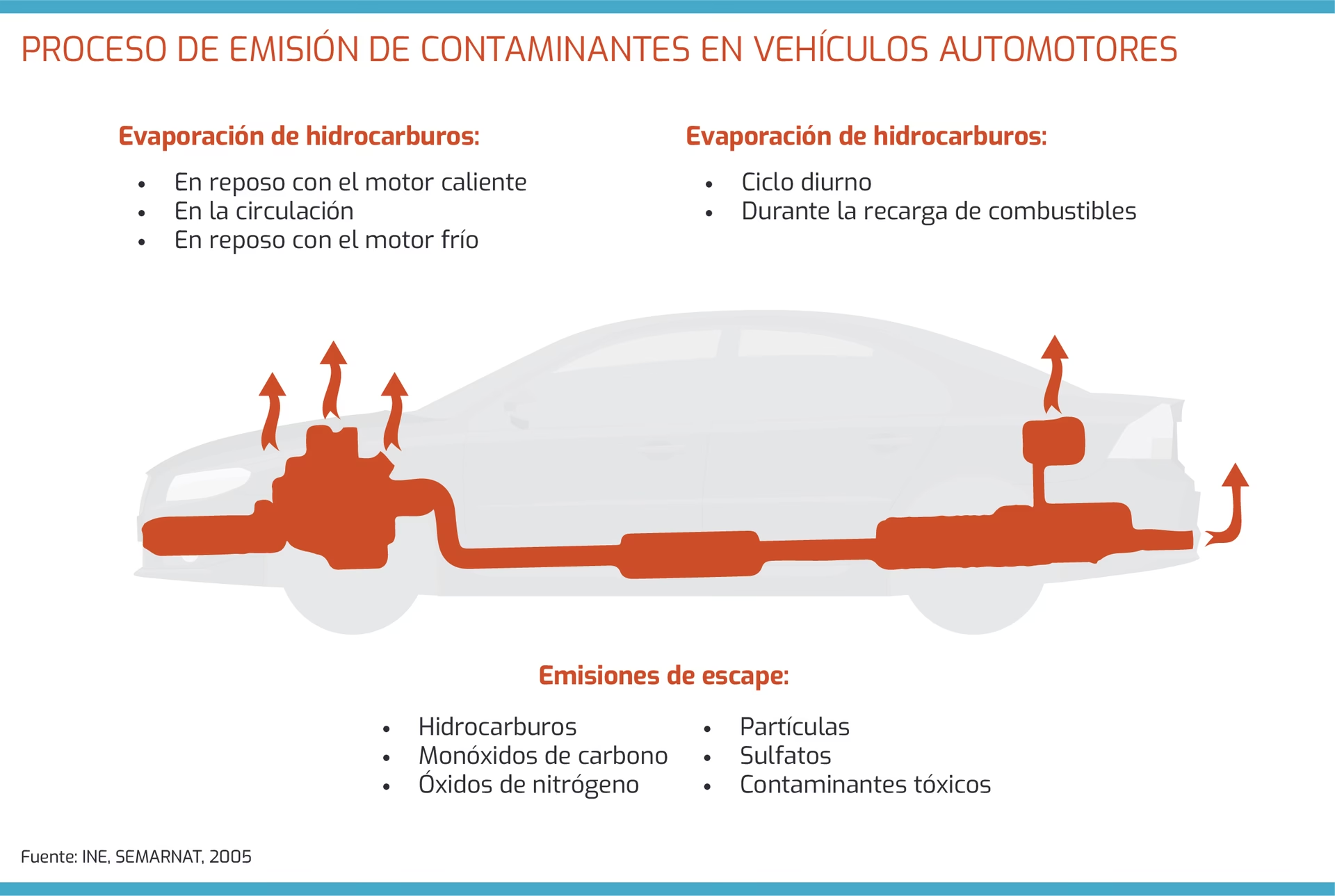
La Combustión de Combustibles: Una Reacción Redox Clave
La combustión, ese proceso que libera la energía almacenada en los combustibles para mover vehículos, generar electricidad o calentar hogares, es un ejemplo fundamental de una reacción redox. En el contexto de los compuestos orgánicos, que son los componentes principales de los combustibles (gasolina, diésel, gas natural, etc.), la definición de oxidación y reducción se puede extender más allá de la simple transferencia de electrones, ya que los compuestos orgánicos suelen ser covalentes y no iónicos.
Para compuestos orgánicos, la oxidación a menudo implica:
- Ganancia de átomos de oxígeno.
- Pérdida de átomos de hidrógeno.
Y la reducción implica lo contrario:
- Pérdida de átomos de oxígeno.
- Ganancia de átomos de hidrógeno.
Consideremos la combustión del metano (CH4), el componente principal del gas natural:
CH4 + 2O2 → CO2 + 2H2O
En esta reacción:
- El carbono en el metano (CH4) pasa de un estado de oxidación de -4 a +4 en el dióxido de carbono (CO2). Ha perdido electrones (o, viéndolo desde la perspectiva orgánica, ha ganado oxígeno y perdido hidrógeno en relación con su estado inicial). El metano se ha oxidado y actúa como agente reductor.
- El oxígeno molecular (O2), que está en estado de oxidación 0, pasa a estado de oxidación -2 en el CO2 y el H2O. Ha ganado electrones. El oxígeno se ha reducido y actúa como agente oxidante.
La combustión de la gasolina (una mezcla compleja de hidrocarburos) o el diésel sigue el mismo principio general: los hidrocarburos (compuestos de carbono e hidrógeno) reaccionan con el oxígeno del aire, oxidándose a dióxido de carbono y agua, mientras que el oxígeno se reduce. Esta transferencia de electrones y átomos libera una gran cantidad de energía en forma de calor y luz, que es aprovechada por los motores de combustión interna.
En esencia, los combustibles almacenan energía en sus enlaces químicos, y la reacción redox de la combustión permite liberar esa energía al reordenar los átomos en productos más estables (CO2 y H2O).
Otros Ejemplos Orgánicos y Bioquímicos
Más allá de la combustión, las reacciones redox son vitales en la química orgánica y bioquímica:
- Oxidación de alcoholes: Los alcoholes pueden oxidarse para formar aldehídos, cetonas o ácidos carboxílicos, dependiendo de la estructura del alcohol y el agente oxidante. Un ejemplo famoso es la oxidación del etanol en el test de alcoholemia con dicromato de potasio (Cr2O72-), donde el etanol se oxida a acetaldehído o ácido acético, y el cromo (VI) naranja se reduce a cromo (III) verde.
- Reducción de aldehídos y cetonas: Estos compuestos pueden reducirse para formar alcoholes. Este proceso es importante en el metabolismo, como la reducción del ácido pirúvico a ácido láctico en los músculos durante el ejercicio intenso.
- Antioxidantes: Como se mencionó, compuestos como la Vitamina C y E actúan como agentes reductores, neutralizando especies oxidantes dañinas en el cuerpo y en los alimentos (evitando la rancidez de las grasas).
Tabla Resumen de Conceptos Clave
| Concepto | Descripción | Cambio en Estado de Oxidación | Transferencia de Electrones |
|---|---|---|---|
| Oxidación | Proceso donde una sustancia pierde electrones. | Aumenta | Pérdida de electrones |
| Reducción | Proceso donde una sustancia gana electrones. | Disminuye | Ganancia de electrones |
| Agente Oxidante | La sustancia que causa la oxidación (ella misma se reduce). | Disminuye | Acepta electrones |
| Agente Reductor | La sustancia que causa la reducción (ella misma se oxida). | Aumenta | Dona electrones |
| Reacción Redox | Proceso químico donde ocurren simultáneamente oxidación y reducción. | Altera estados de oxidación | Hay transferencia neta de electrones |
Preguntas Frecuentes sobre Reacciones Redox y Combustión
¿Por qué la oxidación y la reducción siempre ocurren juntas?
Porque los electrones no pueden simplemente aparecer o desaparecer. Si una sustancia pierde electrones (se oxida), debe haber otra sustancia presente para aceptar esos electrones (reducirse). Es un intercambio necesario.
¿Qué significa el estado de oxidación?
Es una carga hipotética asignada a un átomo en un compuesto, útil para seguir el rastro de los electrones en las reacciones redox. No siempre corresponde a la carga real del átomo, especialmente en compuestos covalentes.
¿El oxígeno es siempre el agente oxidante en una reacción redox?
No siempre, pero el oxígeno es un agente oxidante muy común y potente debido a su alta electronegatividad. En la combustión, el oxígeno molecular (O2) es el oxidante principal.
¿Cómo se identifica si un compuesto orgánico se oxida o se reduce?
Además de calcular los estados de oxidación (lo cual puede ser complejo en moléculas grandes), una regla práctica para compuestos orgánicos es observar los cambios en el contenido de oxígeno e hidrógeno. Ganancia de oxígeno o pérdida de hidrógeno suele indicar oxidación. Pérdida de oxígeno o ganancia de hidrógeno suele indicar reducción.
¿Todas las reacciones que producen energía son redox?
Muchas reacciones energéticas importantes, como la combustión, la respiración y las reacciones en baterías, son redox. Sin embargo, existen reacciones energéticas que no son redox, como algunas reacciones nucleares o cambios de fase.
¿Qué relación tienen las reacciones redox con la corrosión de los autos?
La corrosión del metal en un automóvil, como la formación de óxido en el chasis o la carrocería (generalmente hierro), es una reacción redox. El hierro se oxida (pierde electrones) y el oxígeno del aire, en presencia de agua, se reduce (gana electrones), formando óxido de hierro. Este proceso degrada el material.
¿La energía de la combustión proviene directamente de la transferencia de electrones?
La energía liberada en la combustión proviene de la diferencia en la energía potencial de los enlaces químicos en los reactivos (combustible y oxígeno) y los productos (CO2 y H2O). La transferencia de electrones y el reordenamiento atómico que ocurre en la reacción redox facilitan este cambio de energía, liberando el exceso en forma de calor y luz.
En conclusión, las reacciones redox son pilares de la química que explican cómo se transforma la materia mediante el intercambio de electrones. Desde los procesos biológicos más íntimos hasta la escala industrial de la generación de energía a partir de combustibles, comprender la oxidación y la reducción nos permite apreciar la intrincada danza de los átomos que sustenta nuestro mundo.
Si quieres conocer otros artículos parecidos a Reacciones Redox: El Motor Oculto del Combustible puedes visitar la categoría Automóviles.