19/02/2025
Las baterías son componentes esenciales en nuestra vida moderna, especialmente en el mundo del automovilismo. Son la chispa inicial que pone en marcha el motor, el corazón eléctrico que permite que los sistemas funcionen incluso cuando el vehículo está apagado. Pero, ¿alguna vez te has preguntado qué ocurre realmente dentro de esa caja pesada y sellada? ¿Cómo se genera esa energía eléctrica y, más importante aún, por qué, con el tiempo, todas las baterías parecen tener una vida limitada y finalmente "mueren"?

La respuesta a estas preguntas se encuentra en el fascinante mundo de la química. Una batería es, en esencia, un dispositivo que almacena energía química y la libera en forma de energía eléctrica a través de un proceso controlado. Este proceso se basa en reacciones químicas entre los materiales que componen la batería.
- El Principio Básico: Reacciones Químicas que Generan Electricidad
- ¿Por Qué las Baterías Dejan de Funcionar o "Mueren"?
- La Batería de Automóvil: Un Tipo Específico
- Las Reacciones Químicas Específicas en una Batería de Ácido de Plomo
- El Proceso de Recarga
- La Muerte Definitiva de la Batería de Coche
- Preguntas Frecuentes sobre Baterías de Coche
El Principio Básico: Reacciones Químicas que Generan Electricidad
El funcionamiento fundamental de cualquier batería se basa en la interacción de diferentes sustancias químicas. Cuando una batería está "cargada" y lista para usarse, contiene una serie de productos químicos originales y sin reaccionar. Al conectar un circuito eléctrico a la batería, se permite que los electrones fluyan, y esto desencadena una serie de reacciones químicas internas. Durante estas reacciones, los productos químicos originales se transforman en sustancias diferentes.
Imagina que la batería tiene dos puntos de conexión principales: el ánodo y el cátodo. Estos dos electrodos están inmersos en una solución o pasta llamada electrolito. Cuando la batería está en funcionamiento, se produce una reacción química en el ánodo que libera electrones. Estos electrones no pueden viajar directamente a través del electrolito hasta el cátodo. En su lugar, son forzados a viajar a través del circuito eléctrico externo que está conectado a la batería (el motor de arranque, las luces, etc.).
Mientras los electrones fluyen por el circuito externo, otra reacción química ocurre simultáneamente en el cátodo, donde estos electrones son absorbidos y se incorporan a los productos de esa reacción. Este flujo constante de electrones a través del circuito externo es lo que conocemos como corriente eléctrica, la energía que alimenta los dispositivos conectados.
Este proceso continúa mientras haya productos químicos originales disponibles para reaccionar. La energía se libera a medida que los químicos pasan de un estado de mayor energía potencial (los químicos originales) a un estado de menor energía potencial (los productos de la reacción).
¿Por Qué las Baterías Dejan de Funcionar o "Mueren"?
Ahora que entendemos que la electricidad proviene de la transformación de los químicos originales, la razón por la que una batería muere se vuelve más clara. Una batería deja de funcionar eficazmente cuando los productos químicos originales que participan en las reacciones se han agotado o se han transformado casi por completo en los nuevos productos químicos de la reacción. En este punto, la reacción química no puede continuar a un ritmo suficiente para suministrar la corriente eléctrica necesaria.
Piensa en ello como construir algo con piezas de Lego. Tienes una cantidad limitada de piezas. Una vez que has usado todas tus piezas para construir una casa, la acción de construir se detiene porque no te quedan piezas originales. De manera similar, una vez que los químicos originales de la batería se han consumido, la reacción que produce electrones se detiene.
En este punto, para que la reacción continúe y se produzca más electricidad, tendrías dos opciones principales, dependiendo del tipo de batería. Una opción, comparable a comprar más Legos, sería simplemente reemplazar la batería agotada por una nueva que contenga todos sus químicos originales frescos. La otra opción, comparable a desmontar la casa de Lego para reutilizar las piezas, es invertir la reacción química y regenerar los químicos originales a partir de los productos de la reacción. Esto es precisamente cómo funcionan las baterías recargables.
En las baterías recargables, la aplicación de una corriente eléctrica externa (enchufándola a la red eléctrica del coche o a un cargador) fuerza a los productos de la reacción a revertir su transformación y convertirse de nuevo en los químicos originales, almacenando así energía para ser usada posteriormente. Las baterías no recargables, en cambio, utilizan reacciones químicas que no son fácilmente reversibles en la práctica común, o la estructura física se degrada durante la descarga, impidiendo una recarga eficiente.
La Batería de Automóvil: Un Tipo Específico
Las baterías que usamos comúnmente en los automóviles son un tipo específico conocido como baterías de ácido de plomo. Son robustas, relativamente económicas y capaces de entregar la alta corriente necesaria para arrancar un motor de combustión interna.
Una característica interesante de las baterías de coche es que, aunque las vemos como una sola unidad, en realidad están compuestas internamente por varias baterías más pequeñas, llamadas celdas, conectadas en serie. En una batería de coche estándar de 12 voltios, hay típicamente seis de estas celdas. La conexión en serie significa que el voltaje de cada celda individual se suma al de las demás. Cada celda de una batería de ácido de plomo produce aproximadamente 2 voltios. Por lo tanto, seis celdas en serie suman un total de 12 voltios (6 celdas * 2V/celda = 12V), el voltaje estándar requerido para la mayoría de los sistemas eléctricos de los automóviles.
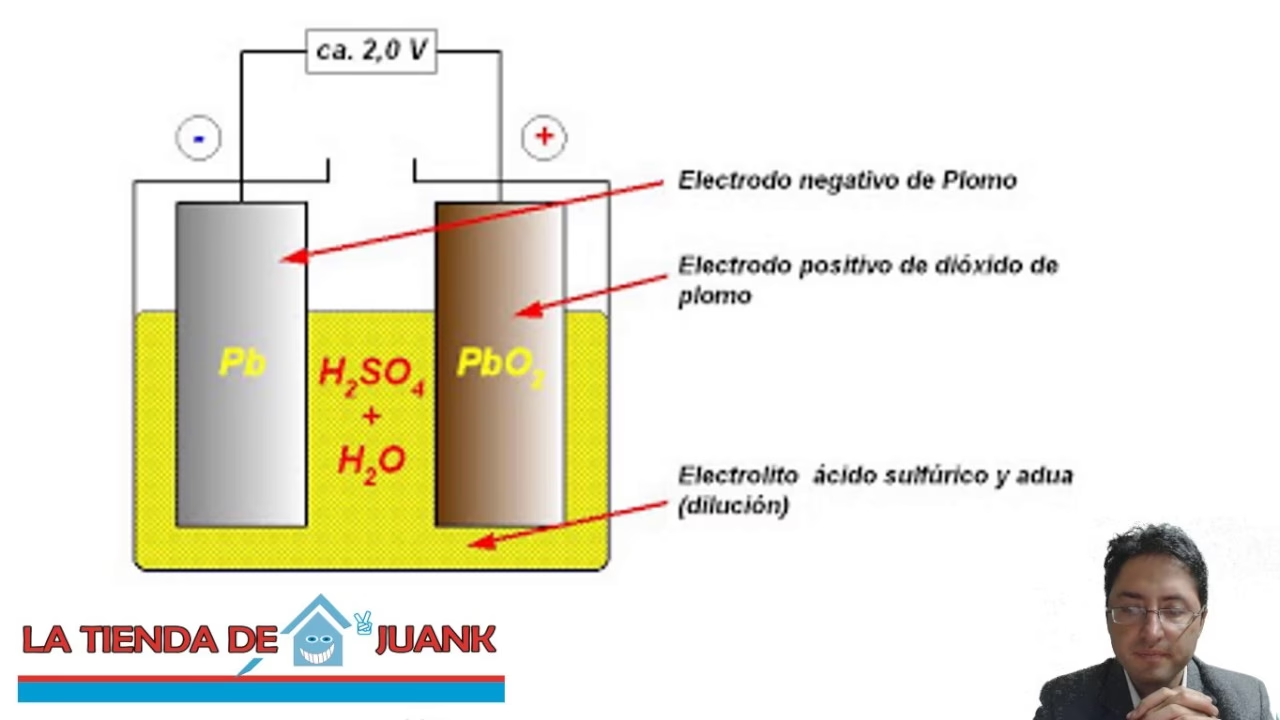
Dentro de cada una de estas seis celdas se encuentran los componentes clave que participan en las reacciones químicas. Como mencionamos, hay un ánodo, un cátodo y un electrolito.
- El ánodo (el electrodo negativo durante la descarga) está hecho de plomo puro en una forma esponjosa y porosa para maximizar la superficie de reacción (Pb).
- El cátodo (el electrodo positivo durante la descarga) está compuesto de dióxido de plomo (PbO₂).
- El electrolito es una solución acuosa de ácido sulfúrico (H₂SO₄).
Estos tres elementos son los protagonistas de las reacciones que generan la electricidad.
Las Reacciones Químicas Específicas en una Batería de Ácido de Plomo
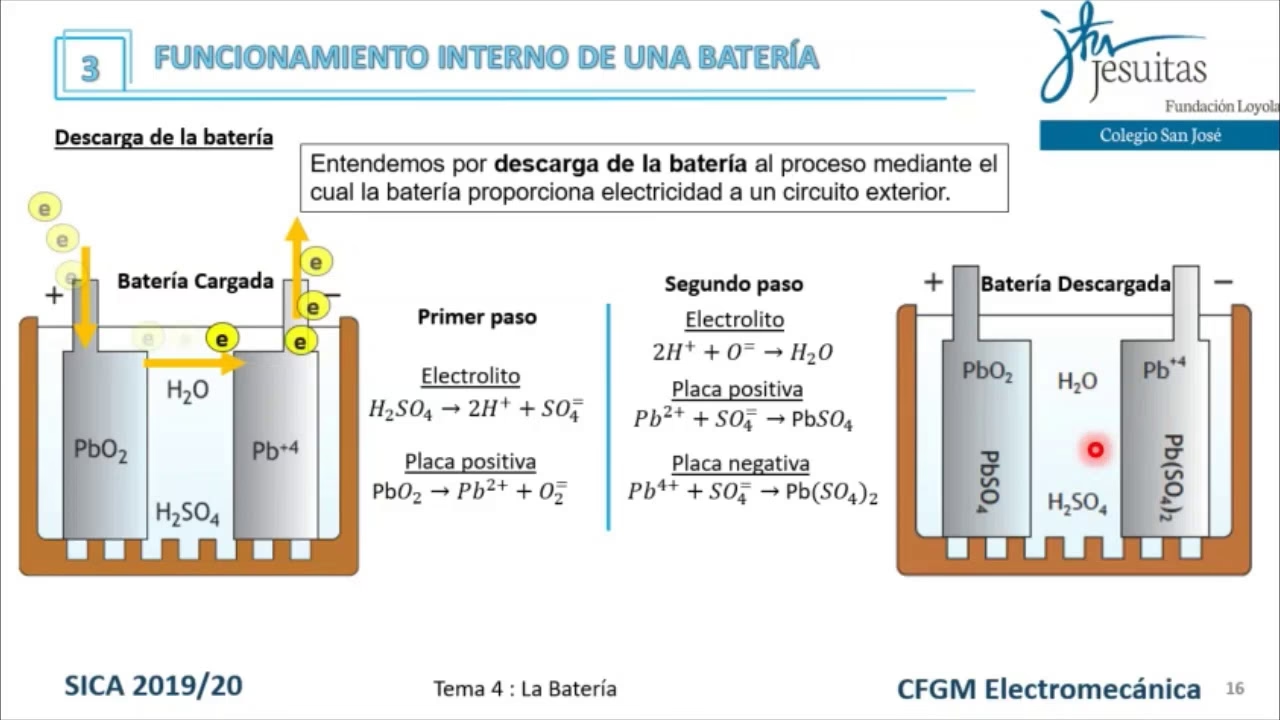
Cuando la batería de un coche se está utilizando (descargando), ocurren las siguientes reacciones químicas principales en el ánodo y el cátodo, facilitadas por el ácido sulfúrico del electrolito:
En el ánodo (plomo esponjoso): El plomo reacciona con los iones sulfato (SO₄²⁻) del ácido sulfúrico.

Pb (s) + SO₄²⁻ (aq) → PbSO₄ (s) + 2e⁻
En esta reacción, el plomo (Pb) se oxida, liberando dos electrones (2e⁻) y formando sulfato de plomo (PbSO₄), que es un sólido que tiende a depositarse en la superficie del ánodo.
En el cátodo (dióxido de plomo): El dióxido de plomo reacciona con los iones hidrógeno (H⁺) y los iones sulfato (SO₄²⁻) del ácido sulfúrico, y con los electrones que llegan desde el circuito externo.
PbO₂ (s) + 4H⁺ (aq) + SO₄²⁻ (aq) + 2e⁻ → PbSO₄ (s) + 2H₂O (l)
Aquí, el dióxido de plomo (PbO₂) se reduce, consumiendo los electrones que han viajado a través del circuito externo y formando también sulfato de plomo (PbSO₄) y agua (H₂O).
Observa que en el ánodo se liberan electrones, mientras que en el cátodo se consumen. Como se mencionó anteriormente, los electrones no pueden cruzar la solución de ácido sulfúrico directamente. Por lo tanto, la única forma en que las reacciones pueden continuar es si los electrones liberados en el ánodo viajan a través del circuito eléctrico externo (para alimentar los componentes del coche) y regresan a la batería para ser consumidos en el cátodo.
La reacción neta global durante la descarga es la suma de estas dos semirreacciones:
Pb (s) + PbO₂ (s) + 2H₂SO₄ (aq) → 2PbSO₄ (s) + 2H₂O (l)
Como resultado de la descarga, tanto el plomo del ánodo como el dióxido de plomo del cátodo se convierten en sulfato de plomo, y el ácido sulfúrico se consume, produciendo agua. Esto disminuye la concentración de ácido sulfúrico en el electrolito.
El Proceso de Recarga
Afortunadamente, la reacción química en una batería de ácido de plomo es reversible. Cuando el alternador del coche (o un cargador externo) suministra energía a la batería, fuerza a los electrones a ir en la dirección opuesta a través del circuito externo. Esto invierte las reacciones químicas:
En el ánodo (ahora se comporta como polo positivo en la recarga):
PbSO₄ (s) + 2e⁻ → Pb (s) + SO₄²⁻ (aq)
El sulfato de plomo se convierte de nuevo en plomo esponjoso.
En el cátodo (ahora se comporta como polo negativo en la recarga):
PbSO₄ (s) + 2H₂O (l) → PbO₂ (s) + 4H⁺ (aq) + SO₄²⁻ (aq) + 2e⁻
El sulfato de plomo se convierte de nuevo en dióxido de plomo.
La reacción neta global durante la recarga es, por lo tanto, la inversa de la descarga:
2PbSO₄ (s) + 2H₂O (l) → Pb (s) + PbO₂ (s) + 2H₂SO₄ (aq)
Durante la recarga, el sulfato de plomo se transforma de nuevo en plomo y dióxido de plomo, y se regenera el ácido sulfúrico, disminuyendo la cantidad de agua y aumentando la concentración de ácido sulfúrico en el electrolito.
La Muerte Definitiva de la Batería de Coche
Aunque la reacción es reversible, el proceso no es perfecto. Cada ciclo de descarga y recarga causa pequeños cambios físicos y químicos irreversibles dentro de las celdas. El principal culpable de la muerte de una batería de coche es la acumulación de sulfato de plomo en una forma cristalina que es difícil o imposible de convertir de nuevo en plomo y dióxido de plomo durante la recarga (sulfatación). Con el tiempo, esta capa de sulfato de plomo endurecido reduce la superficie activa de los electrodos y bloquea la penetración del electrolito, impidiendo que las reacciones químicas ocurran eficientemente. Esto significa que, incluso si hay químicos originales restantes, la batería no puede entregar la corriente necesaria.
Otras causas incluyen la pérdida de material activo de los electrodos, la corrosión interna, o la pérdida de electrolito (en baterías no selladas). Al final, la batería muere porque uno o más de sus componentes clave (plomo, dióxido de plomo, ácido sulfúrico) se han agotado funcionalmente o se han transformado en productos que no pueden participar adecuadamente en las reacciones, o bien la estructura física interna se ha degradado.
Preguntas Frecuentes sobre Baterías de Coche
- ¿Cuánta energía produce cada celda de una batería de coche?
- Cada celda individual en una batería de ácido de plomo de coche produce aproximadamente 2 voltios.
- ¿Por qué una batería de coche es de 12V?
- Una batería de coche estándar de 12V está compuesta por seis celdas de 2V conectadas en serie. La conexión en serie suma los voltajes de cada celda (6 * 2V = 12V).
- ¿Cuáles son los componentes principales de una batería de coche?
- Los componentes químicos activos principales son el ánodo (plomo esponjoso), el cátodo (dióxido de plomo) y el electrolito (una solución de ácido sulfúrico).
- ¿Qué se forma cuando una batería de coche se descarga?
- Cuando una batería de coche se descarga, el plomo y el dióxido de plomo reaccionan con el ácido sulfúrico para formar sulfato de plomo en ambos electrodos y agua.
- ¿Puedo "revivir" una batería muerta?
- Una vez que una batería de ácido de plomo ha sufrido una sulfatación significativa o degradación física, no se puede "revivir" completamente para restaurar su capacidad original. Mientras que la recarga invierte las reacciones, el daño irreversible causado por la sulfatación cristalina y otros factores limita su vida útil. Es como intentar desarmar una casa de Lego donde algunas piezas se han pegado de forma permanente.
Comprender la química detrás de la batería de tu coche no solo es interesante, sino que también te ayuda a entender por qué el mantenimiento adecuado (como evitar descargas profundas) puede prolongar su vida útil. Y cuando finalmente llegue al final de su camino, recuerda que, al igual que reutilizarías tus Legos si pudieras, es importante reciclar tu batería vieja. Los materiales valiosos como el plomo y el ácido sulfúrico pueden ser recuperados y reutilizados, cerrando el ciclo y protegiendo el medio ambiente.
Si quieres conocer otros artículos parecidos a ¿Cómo Funciona y Por Qué Muere una Batería? puedes visitar la categoría Automovilismo.