14/09/2019
El Ciclo de Carnot es una piedra angular en el fascinante campo de la termodinámica. Propuesto por el ingeniero y físico francés Sadi Carnot a principios del siglo XIX, este ciclo no es un diseño de máquina real, sino un modelo teórico idealizado. Su importancia radica en que establece el límite máximo de eficiencia que cualquier máquina térmica puede alcanzar al operar entre dos temperaturas determinadas. Comprender el Ciclo de Carnot es fundamental para analizar el rendimiento de los motores térmicos, las máquinas frigoríficas y otros dispositivos que convierten calor en trabajo o viceversa.
https://www.youtube.com/watch?v=0gcJCdgAo7VqN5tD
La termodinámica, en esencia, estudia la energía y sus transformaciones. Dentro de este estudio, las máquinas térmicas son dispositivos diseñados para convertir energía térmica (calor) en energía mecánica (trabajo). El desafío constante en ingeniería es hacer que esta conversión sea lo más eficiente posible, minimizando las pérdidas de energía. Aquí es donde el Ciclo de Carnot se vuelve invaluable, actuando como un punto de referencia insuperable.
- ¿Por Qué el Ciclo de Carnot es un Modelo Ideal?
- ¿Qué Máquinas se Relacionan con el Ciclo de Carnot?
- El Teorema de Carnot: El Límite Fundamental
- La Fórmula de Eficiencia de Carnot
- Los Cuatro Procesos del Ciclo de Carnot
- Ciclo Real vs. Ciclo Ideal de Carnot
- Preguntas Frecuentes sobre el Ciclo de Carnot
¿Por Qué el Ciclo de Carnot es un Modelo Ideal?
La razón principal por la que el Ciclo de Carnot es considerado ideal es que opera bajo condiciones hipotéticas de reversibilidad. Esto implica que todos los procesos dentro del ciclo son cuasiestáticos (ocurren infinitamente lento, pasando por estados de equilibrio) y libres de irreversibilidades como la fricción, la transferencia de calor a través de diferencias finitas de temperatura o la mezcla de fluidos. En un ciclo de Carnot ideal, no hay pérdidas de energía que no sean inherentes a la conversión de calor en trabajo (o trabajo en calor, en el caso inverso).
Las condiciones ideales del ciclo incluyen:
- Procesos Reversibles: Cada etapa del ciclo puede invertirse, devolviendo tanto el sistema como su entorno a sus estados iniciales sin ningún cambio neto.
- Ausencia de Fricción: No hay pérdidas de energía mecánica debido al rozamiento entre las partes móviles.
- Transferencia de Calor Isoterma: El calor se transfiere hacia o desde el sistema solo cuando está en contacto con fuentes de calor a temperaturas constantes, sin caídas de temperatura finitas.
- Procesos Adiabáticos Perfectos: Las etapas de expansión y compresión sin intercambio de calor son perfectamente aisladas del entorno.
Estas condiciones son imposibles de lograr completamente en la realidad. Las máquinas reales siempre tienen fricción, la transferencia de calor siempre ocurre a través de gradientes de temperatura y los procesos nunca son perfectamente cuasiestáticos o adiabáticos. Sin embargo, el Ciclo de Carnot nos dice cuál es el mejor rendimiento posible bajo ciertas temperaturas de operación, proporcionando una meta teórica para los ingenieros que diseñan máquinas térmicas.
¿Qué Máquinas se Relacionan con el Ciclo de Carnot?
Si bien ninguna máquina real opera *exactamente* según el Ciclo de Carnot ideal, este modelo es fundamental para entender y analizar una amplia variedad de dispositivos térmicos. Las máquinas reales buscan aproximarse a la eficiencia de Carnot tanto como sea posible, reduciendo las irreversibilidades.
Aquí se presentan algunos ejemplos de máquinas y sistemas que se estudian y diseñan utilizando los principios del Ciclo de Carnot como referencia:
Motores de Combustión Interna
Los motores que impulsan la mayoría de los automóviles, camiones y motocicletas operan en ciclos que, aunque difieren significativamente del de Carnot (como el ciclo Otto o el ciclo Diesel), son analizados a menudo comparando su eficiencia real con la eficiencia teórica de un ciclo de Carnot operando entre las temperaturas máxima y mínima alcanzadas en el ciclo real. Los procesos de admisión, compresión, combustión, expansión y escape en un motor de combustión interna implican irreversibilidades (como la combustión rápida, la fricción, las pérdidas de calor) que impiden que alcancen la eficiencia de Carnot. Sin embargo, la comprensión del ciclo ideal ayuda a identificar áreas de mejora, como aumentar la relación de compresión o reducir las pérdidas por fricción.
Turbinas de Vapor (Centrales Termoeléctricas)
Las centrales eléctricas que queman combustibles fósiles o utilizan energía nuclear para generar electricidad a menudo emplean turbinas de vapor. Estas máquinas funcionan calentando agua hasta convertirla en vapor a alta presión y temperatura, que luego se expande a través de una turbina para generar trabajo mecánico (que mueve un generador eléctrico). El vapor se condensa posteriormente para completar el ciclo (como el ciclo Rankine). Aunque el ciclo Rankine también tiene sus propias características y desviaciones del ideal, la eficiencia máxima teórica para una turbina de vapor operando entre la temperatura de la caldera (fuente caliente) y la temperatura del condensador (fuente fría) está limitada por la eficiencia de un ciclo de Carnot entre esas mismas temperaturas. Los ingenieros trabajan para optimizar componentes como las calderas, las turbinas y los condensadores para acercar la eficiencia real a este límite teórico.
Máquinas Frigoríficas y Bombas de Calor
Los refrigeradores y los aires acondicionados son ejemplos de máquinas frigoríficas, que operan en un ciclo inverso al de un motor térmico. En lugar de producir trabajo a partir de calor, utilizan trabajo para transferir calor de una fuente fría a una fuente caliente. Las bombas de calor hacen lo mismo, pero su objetivo principal es transferir calor a un espacio cálido para calefacción. El ciclo de Carnot inverso representa el ciclo ideal para estas máquinas, definiendo el Coeficiente de Rendimiento (COP) máximo posible. Los ciclos de refrigeración reales (como el ciclo de compresión de vapor) utilizan refrigerantes y tienen componentes como compresores, condensadores, válvulas de expansión y evaporadores que introducen irreversibilidades, lo que resulta en un COP real inferior al COP de Carnot inverso.
Células de Combustible y Otros Dispositivos Energéticos
Aunque las células de combustible convierten energía química en eléctrica directamente (sin pasar por un ciclo térmico tradicional), los principios termodinámicos, incluido el concepto de eficiencia limitada por la temperatura, siguen siendo relevantes. El Ciclo de Carnot proporciona un contexto para entender por qué incluso estos sistemas tienen límites de eficiencia, aunque la naturaleza de esos límites difiera de la de las máquinas térmicas puras.
El Teorema de Carnot: El Límite Fundamental
El Teorema de Carnot, derivado del Segundo Principio de la Termodinámica, establece dos afirmaciones cruciales:
- No puede existir una máquina térmica que, operando entre dos focos térmicos dados, tenga un rendimiento mayor que el de una máquina de Carnot que opere entre esos mismos focos.
- Todas las máquinas térmicas reversibles que operan entre los mismos dos focos térmicos tienen el mismo rendimiento, que es igual al de la máquina de Carnot.
La primera parte del teorema es la más impactante para la ingeniería práctica. Significa que, sin importar cuán ingenioso sea el diseño de una máquina térmica o cuál sea la sustancia de trabajo utilizada, su eficiencia nunca podrá superar la de un ciclo de Carnot ideal que opere entre las mismas temperaturas de la fuente caliente (T1) y la fuente fría (T2). Esto establece un límite superior fundamental para la eficiencia.
La segunda parte subraya la universalidad de la eficiencia de Carnot para ciclos reversibles, demostrando que esta eficiencia depende únicamente de las temperaturas de las fuentes de calor.
La Fórmula de Eficiencia de Carnot
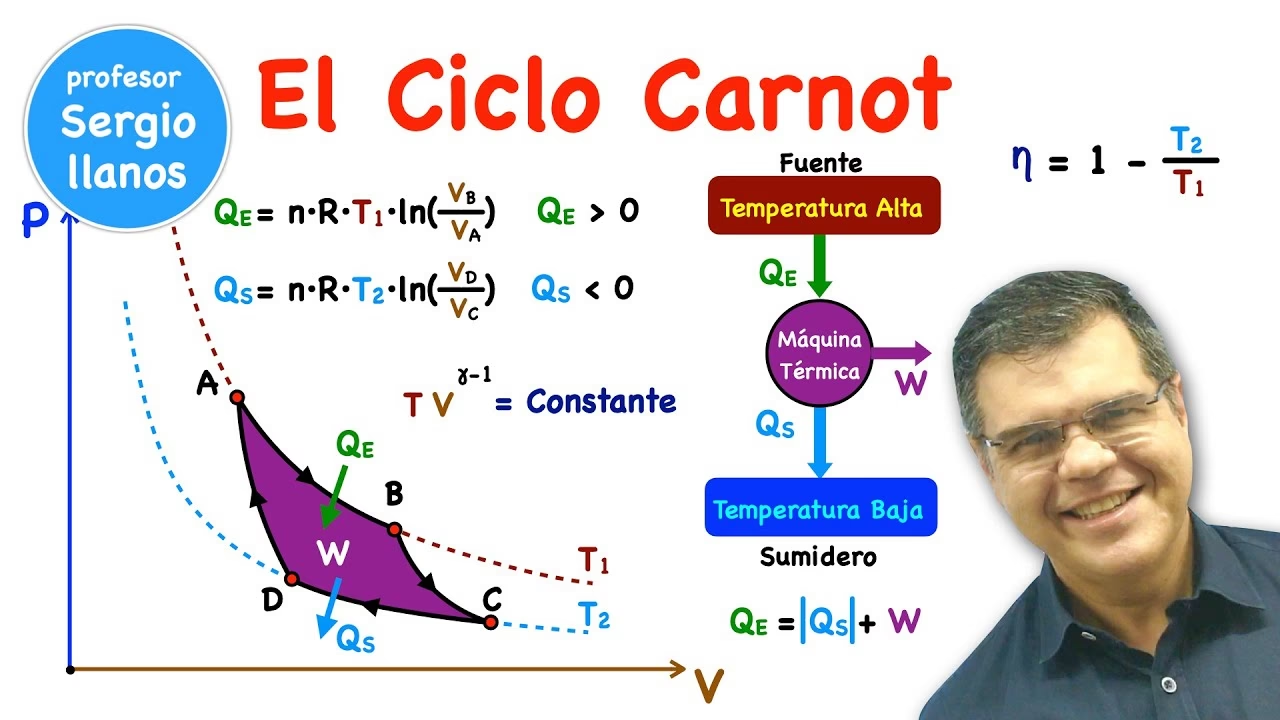
La eficiencia (η) de un ciclo de Carnot (y, por lo tanto, la eficiencia máxima teórica para cualquier máquina térmica operando entre dos temperaturas) se expresa con la siguiente fórmula:
η = 1 - (T₂ / T₁)
Donde:
- η es la eficiencia térmica del ciclo.
- T₁ es la temperatura absoluta de la fuente caliente (en Kelvin).
- T₂ es la temperatura absoluta de la fuente fría (en Kelvin).
Esta fórmula revela un concepto crucial: para maximizar la eficiencia, se debe hacer que la temperatura de la fuente caliente (T₁) sea lo más alta posible y la temperatura de la fuente fría (T₂) sea lo más baja posible. La eficiencia es cero si T₁ = T₂, lo cual tiene sentido, ya que no hay diferencia de temperatura para impulsar el flujo de calor y generar trabajo. La eficiencia se acerca al 100% solo si T₂ se acerca al cero absoluto, lo cual es inalcanzable.
Los Cuatro Procesos del Ciclo de Carnot
El Ciclo de Carnot consta de cuatro procesos termodinámicos reversibles que se realizan sobre una sustancia de trabajo (típicamente un gas ideal) contenida en un cilindro con un pistón. Estos procesos, que forman un ciclo cerrado, son:
1. Expansión Isoterma (A → B)
El sistema (gas) está en contacto con la fuente caliente a temperatura constante T₁. El gas se expande lentamente, realizando trabajo sobre el pistón. A medida que se expande, el gas tiende a enfriarse, pero absorbe calor (Q₁) de la fuente caliente para mantener su temperatura constante. Durante este proceso, la energía interna del gas ideal no cambia (ya que la temperatura es constante), por lo que todo el calor absorbido se convierte en trabajo realizado.
En un diagrama Presión-Volumen (P-V), este proceso se representa como una curva descendente (la presión disminuye a medida que el volumen aumenta) a temperatura constante. En un diagrama Temperatura-Entropía (T-S), es una línea horizontal hacia la derecha (temperatura constante, entropía aumenta debido a la absorción de calor).
2. Expansión Adiabática (B → C)
El sistema se aísla térmicamente (no hay intercambio de calor con el exterior). El gas continúa expandiéndose, realizando más trabajo. Al no recibir calor, la energía necesaria para este trabajo proviene de la energía interna del gas, lo que provoca que su temperatura disminuya desde T₁ hasta T₂. Este proceso continúa hasta que el gas alcanza la temperatura de la fuente fría.

En el diagrama P-V, es una curva descendente más pronunciada que la isoterma. En el diagrama T-S, es una línea vertical hacia abajo (entropía constante, temperatura disminuye).
3. Compresión Isoterma (C → D)
El sistema se pone en contacto con la fuente fría a temperatura constante T₂. Se aplica trabajo externo para comprimir lentamente el gas. A medida que se comprime, el gas tiende a calentarse, pero cede calor (Q₂) a la fuente fría para mantener su temperatura constante. Al igual que en la expansión isoterma, la energía interna del gas ideal no cambia.
En el diagrama P-V, es una curva ascendente (la presión aumenta a medida que el volumen disminuye) a temperatura constante. En el diagrama T-S, es una línea horizontal hacia la izquierda (temperatura constante, entropía disminuye debido a la cesión de calor).
4. Compresión Adiabática (D → A)
El sistema se aísla térmicamente de nuevo. El gas se sigue comprimiendo. Como no puede ceder calor, el trabajo realizado sobre el gas durante esta compresión aumenta su energía interna, elevando su temperatura desde T₂ hasta T₁. Este proceso continúa hasta que el gas regresa a su estado inicial (volumen mínimo y temperatura T₁), completando el ciclo.
En el diagrama P-V, es una curva ascendente más pronunciada que la isoterma, regresando al punto de partida. En el diagrama T-S, es una línea vertical hacia arriba (entropía constante, temperatura aumenta), también regresando al punto de partida.
El trabajo neto realizado por el ciclo es el área encerrada por los cuatro procesos en el diagrama P-V. En un ciclo de motor, este trabajo neto es positivo (se produce trabajo). En un ciclo de refrigeración (Ciclo de Carnot inverso), el trabajo neto es negativo (se requiere trabajo).
Ciclo Real vs. Ciclo Ideal de Carnot
La principal diferencia entre un ciclo real y el ciclo ideal de Carnot radica en la presencia de irreversibilidades en los procesos reales. Estas irreversibilidades pueden ser de varios tipos:
- Fricción: El movimiento de las partes mecánicas siempre genera fricción, que disipa energía.
- Transferencia de Calor con Diferencia Finita de Temperatura: Para que el calor fluya a una velocidad práctica, debe haber una diferencia de temperatura finita entre el sistema y la fuente, lo cual es irreversible. Los procesos isotérmicos ideales de Carnot asumen una diferencia de temperatura infinitesimal.
- Expansión o Compresión Rápidas: Los procesos reales no son cuasiestáticos. La expansión o compresión rápidas generan gradientes de presión y temperatura dentro del sistema que no permiten alcanzar estados de equilibrio.
- Mezcla de Fluidos: Si hay mezcla de fluidos a diferentes temperaturas o presiones, esto introduce irreversibilidades.
- Pérdidas de Calor al Entorno: Las paredes de los cilindros o tuberías nunca son perfectamente adiabáticas, lo que provoca pérdidas de calor no deseadas.
Debido a estas irreversibilidades, el trabajo neto producido por una máquina térmica real es siempre menor que el de una máquina de Carnot operando entre las mismas temperaturas de fuente caliente y fría. De manera equivalente, la eficiencia real (ηreal) de cualquier máquina térmica es siempre menor que la eficiencia de Carnot (ηCarnot = 1 - T₂/T₁).
ηreal < ηCarnot
Esta desigualdad es una consecuencia directa del Teorema de Carnot y del Segundo Principio de la Termodinámica. Significa que, aunque el Ciclo de Carnot es un objetivo inalcanzable, sirve como un punto de referencia fundamental para evaluar el rendimiento de las máquinas térmicas existentes y guiar los esfuerzos para mejorarlas.
Preguntas Frecuentes sobre el Ciclo de Carnot
Para clarificar aún más el concepto, abordemos algunas preguntas comunes:
¿Qué máquinas usan el Ciclo de Carnot?
Ninguna máquina real usa el Ciclo de Carnot en su forma ideal. El Ciclo de Carnot es un modelo teórico. Sin embargo, los principios y el análisis basados en el Ciclo de Carnot se aplican al estudio y diseño de máquinas térmicas reales como motores de combustión interna, turbinas de vapor, máquinas frigoríficas (refrigeradores y aires acondicionados) y bombas de calor. Estas máquinas reales operan en ciclos termodinámicos que se comparan con el ciclo de Carnot para entender sus límites de eficiencia.
¿Es real una máquina de Carnot?
No, una máquina de Carnot es una máquina ideal, no una máquina real. Se basa en procesos termodinámicos reversibles (expansiones y compresiones isotérmicas y adiabáticas perfectas) que son imposibles de lograr en la práctica debido a la existencia inevitable de irreversibilidades como la fricción, la transferencia de calor no ideal y la velocidad finita de los procesos.
¿Cuál es la máquina más eficiente del mundo?
Según el Teorema de Carnot, la máquina térmica más eficiente posible operando entre dos temperaturas dadas sería una máquina de Carnot. Su eficiencia es el límite superior teórico. En el mundo real, la eficiencia de cualquier máquina siempre será menor que la de Carnot. No existe una única "máquina más eficiente del mundo" en términos absolutos; la eficiencia real depende del tipo de máquina, su diseño, las temperaturas de operación y cómo se gestionan las irreversibilidades. Sin embargo, las grandes centrales eléctricas modernas, particularmente las de ciclo combinado, logran eficiencias relativamente altas en comparación con otros motores térmicos.
¿Cuáles son los 4 ciclos de Carnot?
No existen "4 ciclos de Carnot". El Ciclo de Carnot es un único ciclo termodinámico compuesto por cuatro procesos o etapas. Estas cuatro etapas son: 1) Expansión Isoterma, 2) Expansión Adiabática, 3) Compresión Isoterma, y 4) Compresión Adiabática. Estos cuatro procesos se suceden en un orden específico para completar el ciclo.
En resumen, aunque el Ciclo de Carnot es un concepto teórico y no se implementa directamente en máquinas reales, su importancia es innegable. Proporciona el marco para comprender los límites fundamentales de la eficiencia de la conversión de energía térmica y sirve como una herramienta esencial para el análisis y la mejora de las máquinas térmicas y frigoríficas que impulsan gran parte de nuestra tecnología moderna.
Si quieres conocer otros artículos parecidos a ¿Qué Máquinas Usan el Ciclo de Carnot? puedes visitar la categoría Automóviles.
